文献解读
Nat Metab|一碳代谢:肌肉挥霍能量&癌症恶病质的核心推手
恶病质是一种影响大多数癌症患者的多因素消耗性疾病,会导致患者出现体重和肌肉量下降,而这种消耗无法通过常规的营养补充加以纠正。近年研究发现,恶病质涉及肿瘤、肝脏、肌肉和脂肪组织等多器官的协调反应。一般认为,肿瘤分泌的因子(如白细胞介素6,IL-6)通过对宿主靶组织进行代谢重编程,启动恶性循环,最终导致机体消耗。在此过程中,循环代谢物发生显著改变,可有效区分体重稳定与体重下降的癌症患者,凸显其作为诊断和预测性生物标志物的潜力。然而,目前多数研究仍集中于单一组织,整合多组织代谢组学与代谢示踪数据的系统性研究较为匮乏,限制了临床对该疾病状态的整体了解和干预治疗。
2026年1月,海德堡大学医院Maria Rohm、捷克科学院生理学研究所Ondrej Kuda在NatureMetabolism上发表题为“Multi-omics profiling of cachexia-targeted tissues reveals a spatio-temporally coordinated response to cancer”的研究论文。该研究追踪了恶病质进展过程中8个靶向组织的代谢通路动态变化,发现一碳代谢在其中扮演核心角色,与炎症、肌肉葡萄糖高代谢及萎缩密切相关,且这一代谢重塑现象具有普遍性。
技术路线

研究结果
●恶病质重塑宿主多组织特异性代谢谱
研究者首先利用C26结肠癌恶病质小鼠模型对多个组织及肿瘤进行了代谢组学分析。结果显示,恶病质小鼠的血浆、肝脏和脂肪组织呈现出独特的代谢谱,而肌肉和心脏的代谢变化则更为复杂。非恶病质肿瘤未引起宿主组织的显著代谢改变,表明观察到的代谢紊乱主要由恶病质诱导性肿瘤驱动。此外,在癌前恶病质期,部分组织中已可检出代谢物改变,呈现出向恶病质演进的趋势。进一步的聚类分析显示,恶病质组织的代谢谱与非恶病质组织形成独立聚类,其中氨基酸、核苷及相关化合物表现出协同性调控模式。
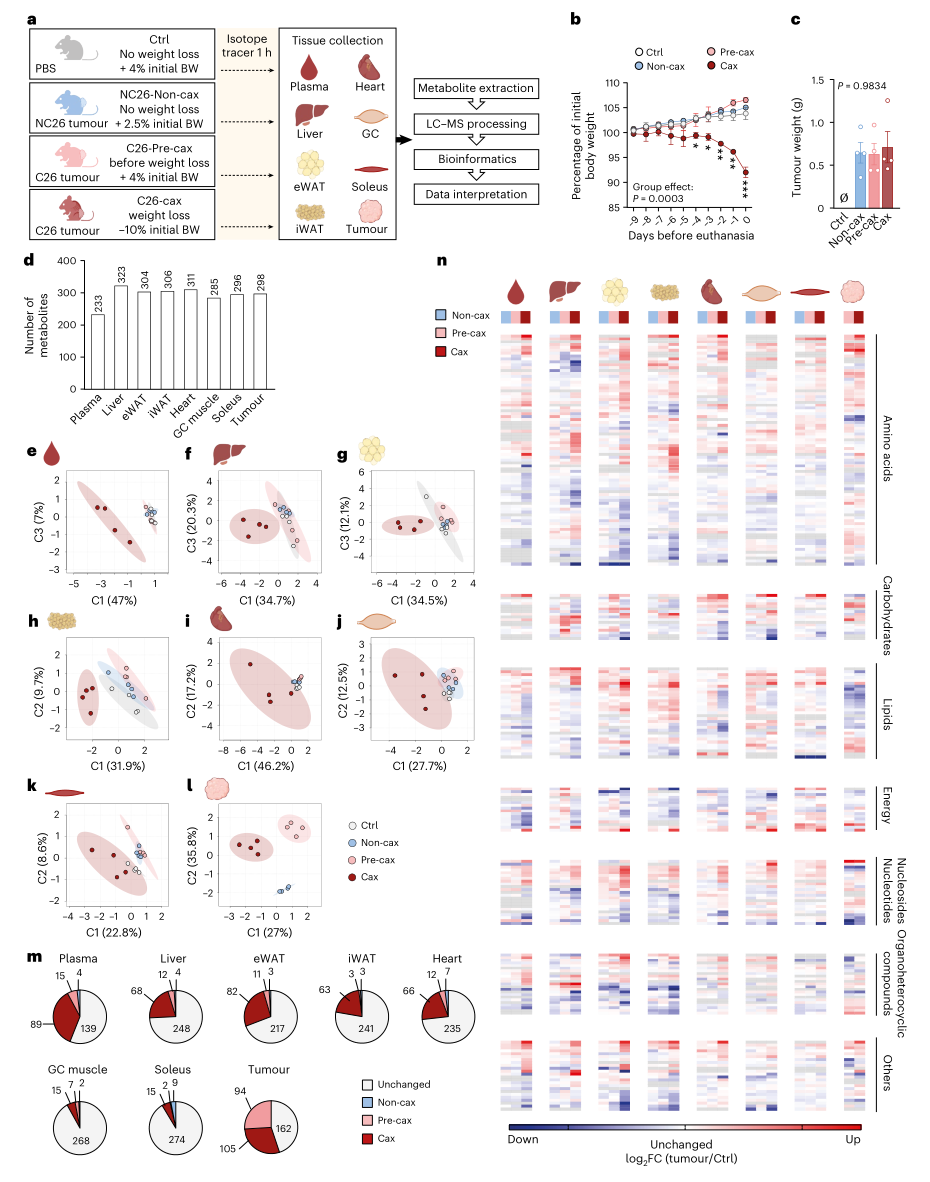
图1. C26恶病质小鼠模型的多组织代谢组学揭示恶病质特异性代谢谱的显著改变
以上结果表明,恶病质并非单一器官的病变,而是引发全身性、组织特异且协调的代谢应答。
●一碳代谢是恶病质中被协同增强的核心跨组织通路
为追踪恶病质进程中代谢物的动态变化,研究者构建了模拟疾病进展(Ctrl→Pre-cax→Cax)的拟时序列分析。结果显示,氨基酸、核苷等代谢物在恶病质发展过程中呈现逐渐增加的趋势,尤其是肌氨酸、三甲基赖氨酸等甲基化氨基酸显著升高;而能量相关代谢物则普遍减少,进一步证实了恶病质中的能量缺乏状态。
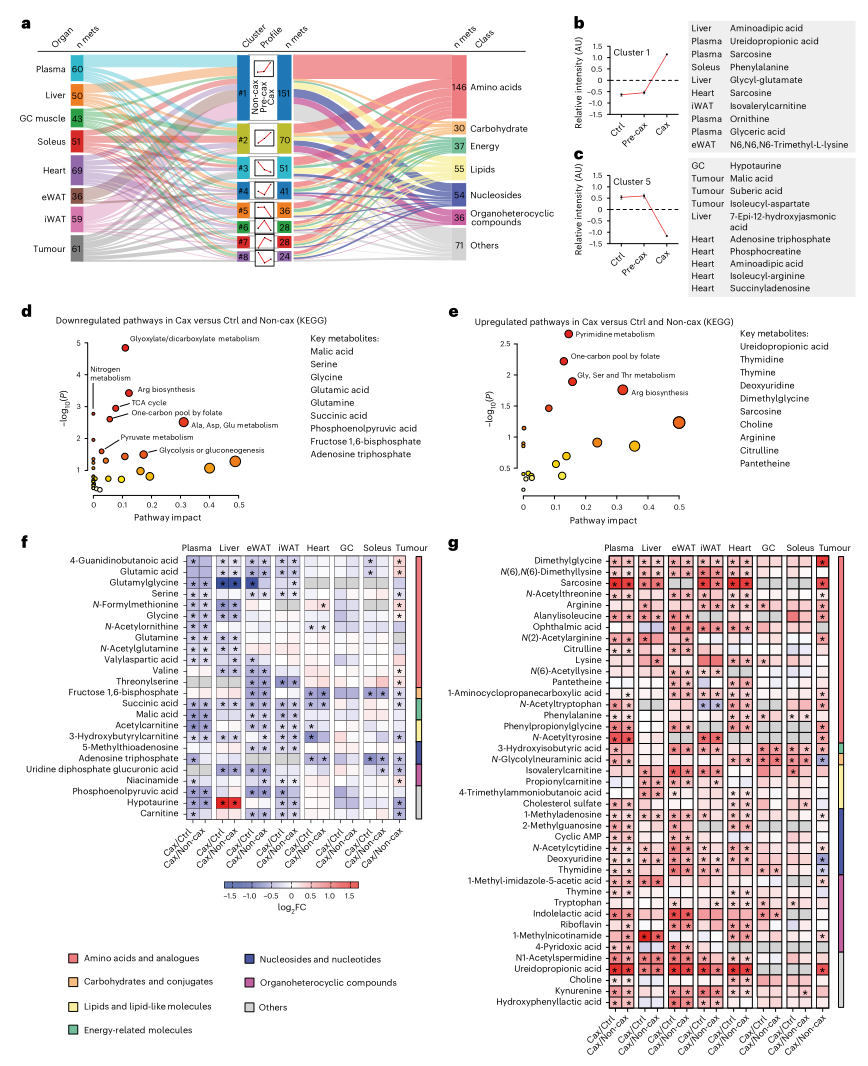
图2. 多组织代谢组学揭示恶病质小鼠中一碳代谢的协同性增强
随后,研究者筛选出在多个组织中共同变化的代谢物,结果发现能量代谢通路的物质普遍下调,且循环氨基酸被大量消耗,这与已知的恶病质特征一致。与之相对,一碳代谢相关产物(如肌氨酸、胸苷等)在恶病质中显著增加。进一步对一碳代谢网络的相关物质进行系统评估后发现,该通路的产物,包括肌氨酸、1-甲基烟酰胺(MNAM)、甲基赖氨酸等甲基化产物,在恶病质小鼠的所有组织及肿瘤中均显著升高,并呈现出组织特异性分布。
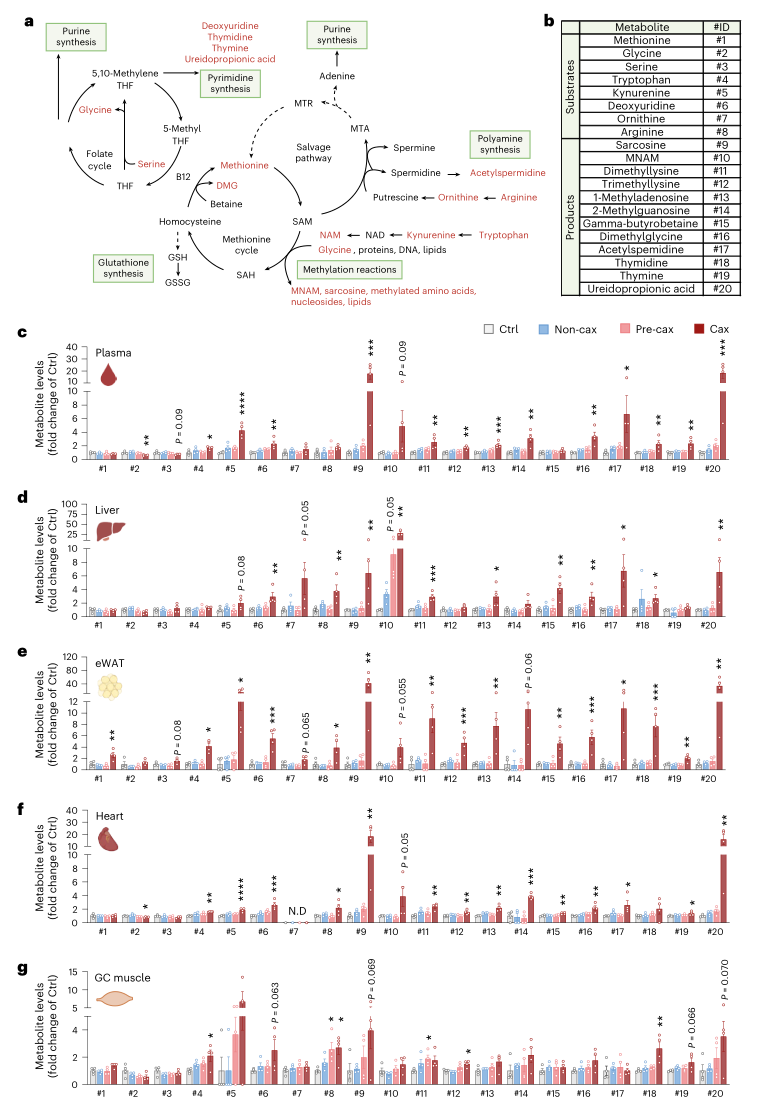
图3. 所有宿主组织中一碳代谢的多种底物和产物均显著增加
以上结果表明,一碳代谢是恶病质中的一个被系统性激活的跨组织共性通路。
●炎症因子IL6驱动恶病质中一碳代谢的转录与代谢重编程
为揭示上述代谢重塑的分子机制,研究者对同一批动物的组织进行了转录组测序。结果显示,恶病质小鼠表现出强烈的转录重塑,激活的通路主要涉及氨基酸代谢、蛋白质合成及翻译后修饰,其中包含编码一碳代谢关键酶的基因;而被抑制的通路则主要与线粒体功能和能量产生相关。整合多组学分析进一步确认一碳代谢是核心改变之一。关键酶基因的表达呈现组织特异性,与代谢物的分布高度吻合。
上游调节因子分析提示炎症反应是这些代谢变化的主要驱动因素。进一步验证发现,无论通过IL6中和抗体处理还是基因敲除,均可显著抑制荷瘤小鼠组织中一碳代谢关键基因的异常表达,并几乎完全消除相关代谢产物的富集。
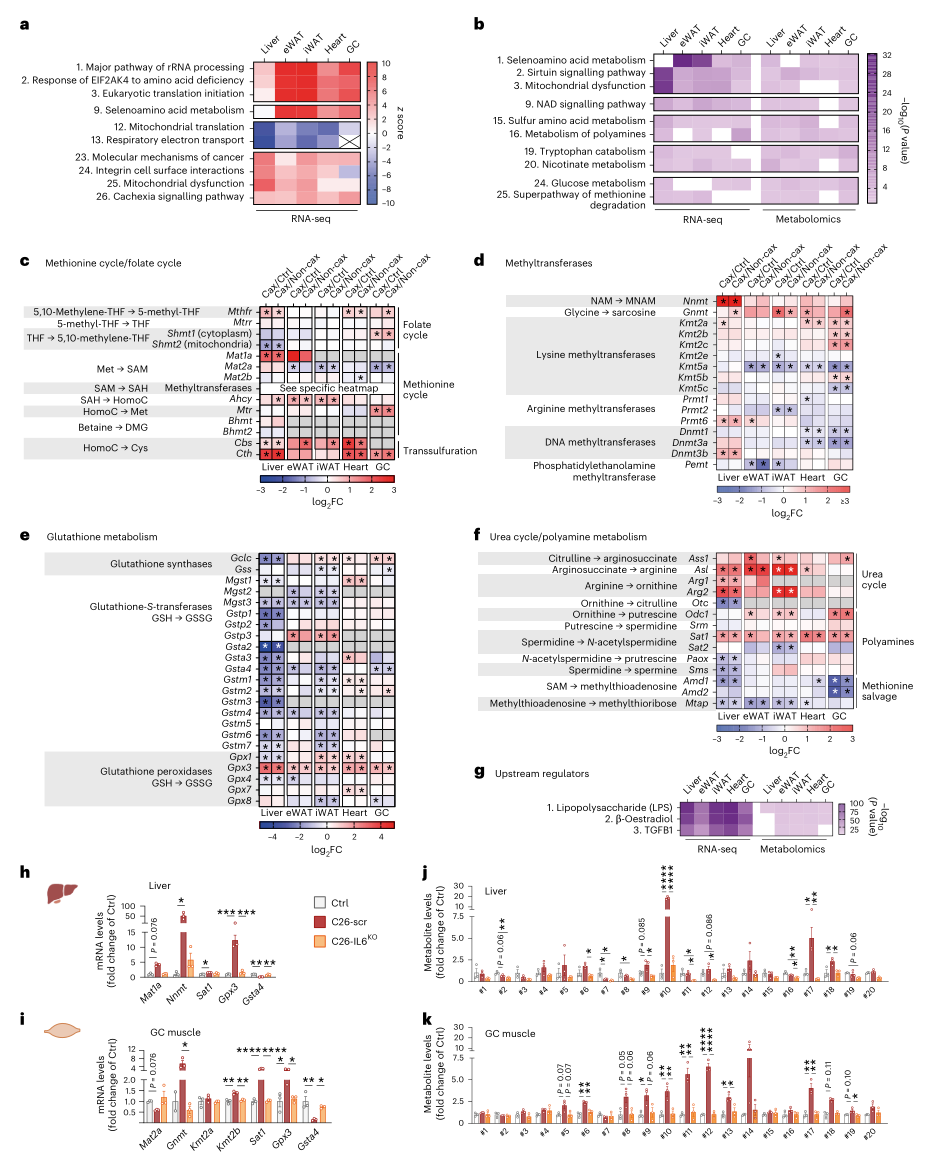
图4. 多组学整合鉴定出在IL6控制下的恶病质相关代谢重编程的关键节点
以上结果证明,肿瘤引发的炎症反应,特别是IL6,是驱动恶病质中一碳代谢系统性激活的关键上游调控节点。
●甲硫氨酸循环过度激活诱导肌管萎缩和代谢亢进
为建立一碳代谢激活与恶病质表型之间的功能联系,研究者在C2C12肌管中进行了体外实验,发现用L-甲硫氨酸激活一碳代谢会诱导肌管萎缩,并伴随葡萄糖消耗增加和代谢亢进状态。13C-葡萄糖示踪实验进一步证实,甲硫氨酸处理导致进入三羧酸循环的葡萄糖通量显著增加,且更高标记同位素体的比例上升,表明葡萄糖被更彻底地氧化以应对能量需求。反之,阻断甲硫氨酸循环则产生相反的表型,且能有效拮抗IL6诱导的肌管萎缩。在脂肪细胞中未观察到类似现象,表明该效应具有肌肉细胞特异性。
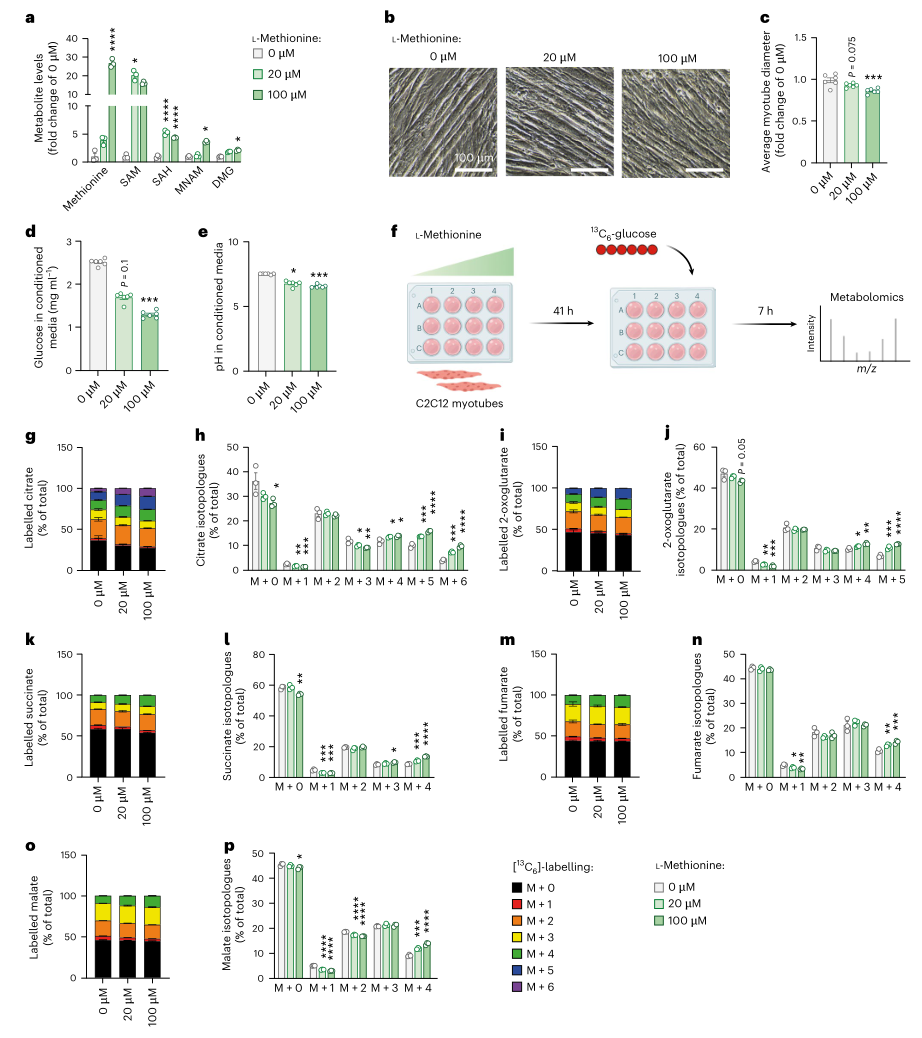
图5. 甲硫氨酸循环的过度激活驱动肌管萎缩和代谢功能障碍
以上结果表明,甲硫氨酸循环的过度激活是一个耗能过程,足以在肌肉细胞中直接驱动代谢亢进和萎缩。
●一碳代谢激活重塑骨骼肌和心肌的葡萄糖代谢
基于体外实验证实的一碳代谢激活可驱动肌肉代谢亢进这一发现,研究者进一步在恶病质小鼠模型中通过13C-葡萄糖示踪技术,验证该机制是否在体内真实存在。结果显示,在肝脏和血浆中,三羧酸循环代谢物的总量和标记量均降低,提示线粒体功能受损;然而在骨骼肌和心肌中,尽管基础代谢物水平不变甚至降低,但三羧酸循环代谢物(如柠檬酸、琥珀酸、延胡索酸和苹果酸)的M+3标记率却显著增加,提示丙酮酸羧化酶(PC)活跃。代谢通量分析进一步证实,恶病质肌肉中进入三羧酸循环的葡萄糖通量增加,而脂肪酸氧化的贡献减少,这一体内表型与体外激活一碳代谢所诱导的代谢变化高度一致。值得注意的是,在癌前恶病质期,肌肉中已出现通量增加的趋势,提示葡萄糖代谢亢进可能是恶病质发生的早期事件。
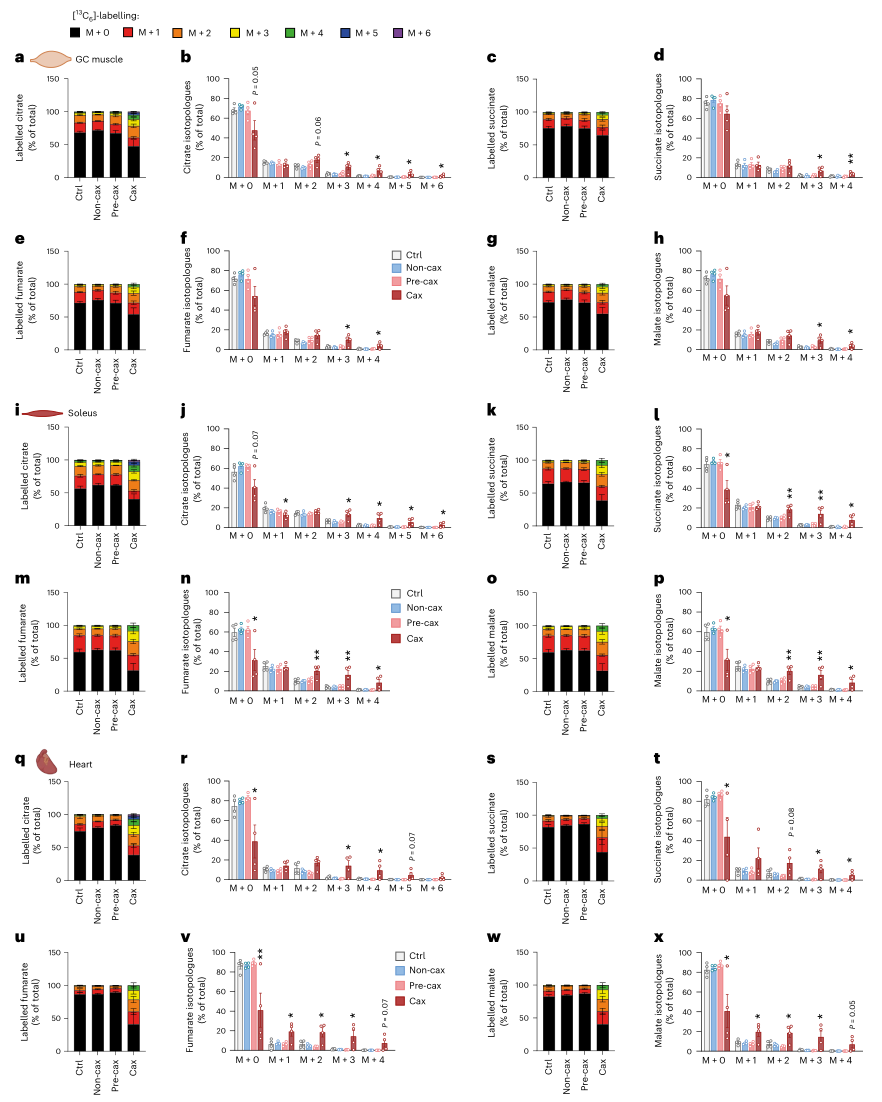
图6. 恶病质引起骨骼肌和心肌中葡萄糖通量的重编程
以上结果表明,在整体能量匮乏的背景下,一碳代谢的系统性激活使恶病质肌肉在接收到营养信号时过度消耗葡萄糖,从而加速了能量耗竭和组织萎缩。
●一碳代谢激活是多种癌症恶病质模型的保守特征,并具有临床相关性
为验证上述发现的普适性,研究者在另外五种独立的小鼠癌症恶病质模型(ApcMin、LLC、KPP、Panc02、8025)中进行了验证。尽管这些模型的肿瘤类型、遗传背景及恶病质发展速度各异,但在所有模型的肝脏和/或肌肉中均观察到与C26模型高度一致的一碳代谢相关基因表达改变及代谢物水平升高,且改变程度与恶病质严重程度呈正相关。此外,在Panc02和8025荷瘤小鼠的肌肉中,同样复现了13C-葡萄糖示踪下三羧酸循环通量增加的现象。
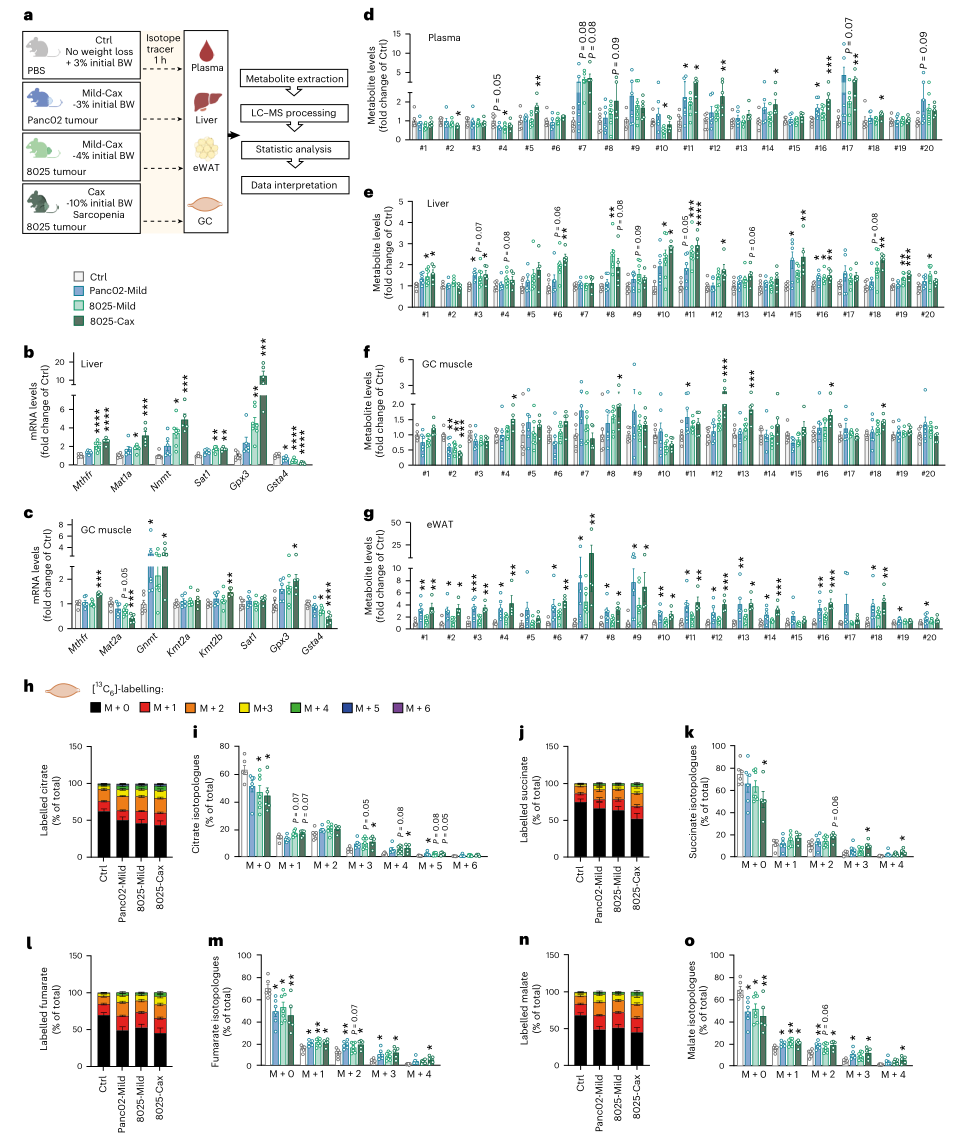
图7. 一碳代谢的激活是小鼠癌症恶病质的共同特征
这些跨模型的保守性改变强有力地证明,一碳代谢的系统性激活是癌症恶病质的核心标志。
为进一步评估其临床相关性,研究者检测了伴有肌肉减少症的癌症患者肝脏和骨骼肌样本,发现NNMT等一碳代谢关键酶基因的表达显著增加。同时,在携带人源SW480结肠癌的恶病质小鼠模型中,完整复现了前述主要发现,包括一碳代谢相关基因表达改变、代谢物水平升高以及肌肉组织中的葡萄糖代谢亢进。
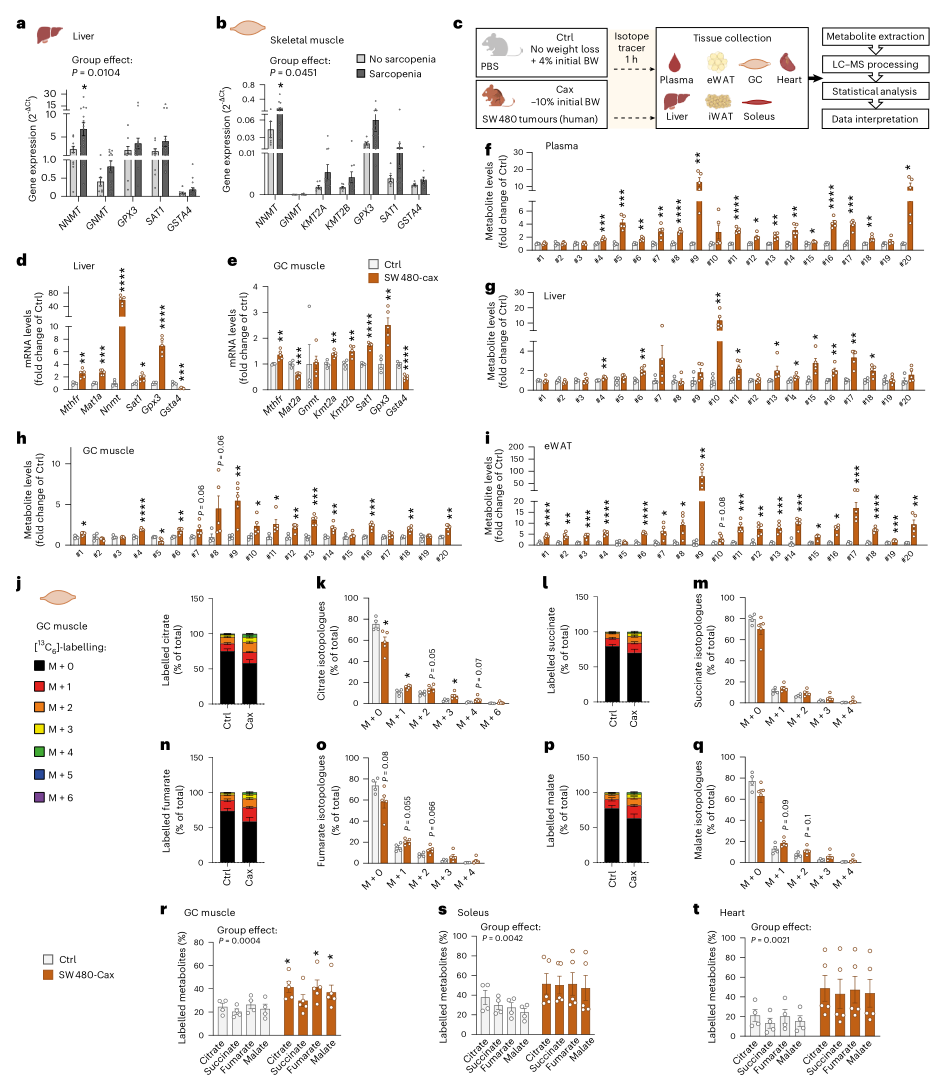
图8. 一碳代谢激活伴随肌肉代谢亢进也是人源化SW480肿瘤小鼠模型恶病质的特征
以上结果提示,一碳代谢激活及伴随的肌肉代谢亢进可能是人类癌症恶病质的关键病理机制,具有重要的临床转化潜能。
全文总结
本研究通过整合代谢组学、RNA测序及13C-葡萄糖示踪代谢流技术,对C26荷瘤雄性小鼠在不同疾病阶段的多组织及肿瘤进行检测,系统揭示了恶病质发生发展过程中的时空代谢重编程特征。结果发现,一碳代谢是啮齿类动物和人类患者代谢消耗的跨组织共性通路,并与炎症反应、葡萄糖代谢亢进及肌肉萎缩密切相关。
本研究构建了癌症恶病质进程中代谢重编程及多组织代谢物协调反应的分子机制框架,揭示一碳代谢作为跨组织共性机制与消耗状态密切相关。
参考文献
Morigny P, Vondrackova M, Ji H, et al. Multi-omics profiling of cachexia-targeted tissues reveals a spatio-temporally coordinated response to cancer. Nat Metab. 2026.
请扫描二维码阅读原文

绘谱帮你测
麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱已为数百家三甲医院、科研院所和企业提供多组学一站式整体解决方案,协助客户与合作伙伴发表SCI文章600+篇,累计影响因子6000+,平均IF>10,涵盖Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等顶级期刊。


