文献解读
客户案例 | GUT:结肠炎患者福音!肠道高丰度Parasutterella菌+免疫陷阱=肠癌高风险,靶向干预有了新方向!
溃疡性结肠炎(UC)是一种让人长期受困扰的慢性炎症性肠病(IBD),肠道黏膜持续受损、免疫应答紊乱失调,不仅让患者饱受不适,还会显著拉高结肠炎相关结直肠癌(CAC)的发病风险。根源在肠道里的菌群失衡,尤其是变形菌门的细菌,已经成为 UC 和 CAC 的核心特征——但这一门里到底哪种 “坏细菌” 在作祟、它们如何悄悄搞破坏,至今还是个没解开的谜。
2025年12月,华南理工大学附属第二医院、广州中医药大学附属第二医院研究团队在Gut上在线发表了题为“Parasutterella excrementihominis exacerbates experimental colitis and colitis-associated colorectal cancer via pathogenic NETosis activation”的研究文章,通过多组学+模型验证,系统阐明了“肠道菌 Parasutterella excrementihominis→代谢物(6-HHA与Suc)→GPR84/SUCNR1→GSDMD依赖性 NETosis→UC/CAC 加重”的完整因果链,P. excrementihominis 及代谢物可作为“活动度+癌变风险”双预测生物标志物。(麦特绘谱提供非靶+16S检测服务)
知识小卡片
NETosis是中性粒细胞活化后启动的一种特殊程序性细胞死亡相关过程,核心是中性粒细胞通过一系列分子调控,将自身核染色质、胞质内的抗菌蛋白(如髓过氧化物酶MPO、中性粒细胞弹性蛋白酶NE)等物质释放到细胞外。
中性粒细胞胞外诱捕网(NETs,Neutrophil Extracellular Traps)是中性粒细胞活化后释放的网状结构,通过活性氧(ROS)和炎症介质加剧UC黏膜损伤,但触发NETs形成的微生物诱因尚未明确。
Gasdermin D(GSDMD)是焦亡相关蛋白,在 NETs 形成和损伤相关分子模式(DAMPs)释放中起关键作用,其依赖的NETosis与慢性炎症疾病进展密切相关。
研究思路
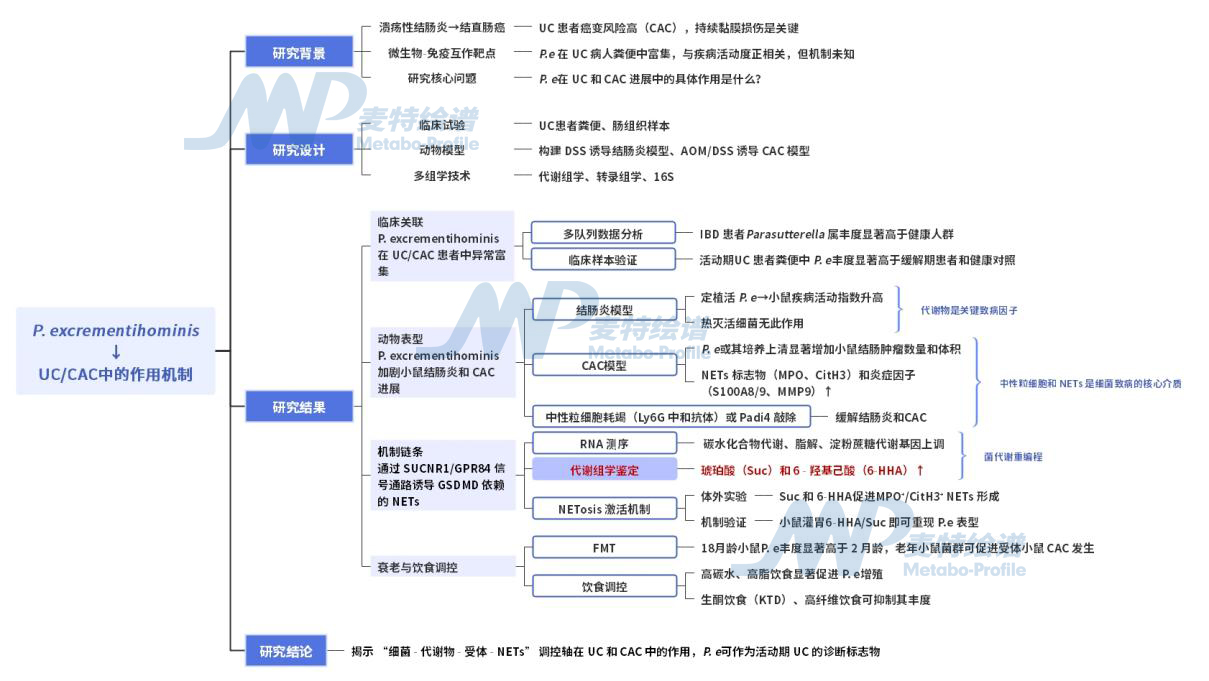
图1. 技术路线
二、研究结果
1、P. excrementihominis在UC患者中异常富集
多队列数据库分析(含4个IBD数据集)显示,IBD 患者(含UC)粪便中Parasutterella属丰度显著高于健康人群,其中在活动期IBD患者中P. excrementihominis的富集特征尤为明显。
临床样本验证进一步证实,115例UC患者(36例缓解期、79例活动期)中,活动期患者粪便P. excrementihominis丰度显著高于缓解期患者及 20 例健康对照。且P. excrementihominis丰度随UC 疾病持续时间延长而升高,在合并CAC的患者中也呈高表达趋势;FISH检测及组织样本分析表明,该细菌在活动期UC患者的炎症结肠黏膜中形成聚集簇,而在缓解期患者黏膜中稀缺或缺失,且炎症区域的细菌丰度显著高于非炎症区域,证实其与UC 疾病严重程度的紧密关联。
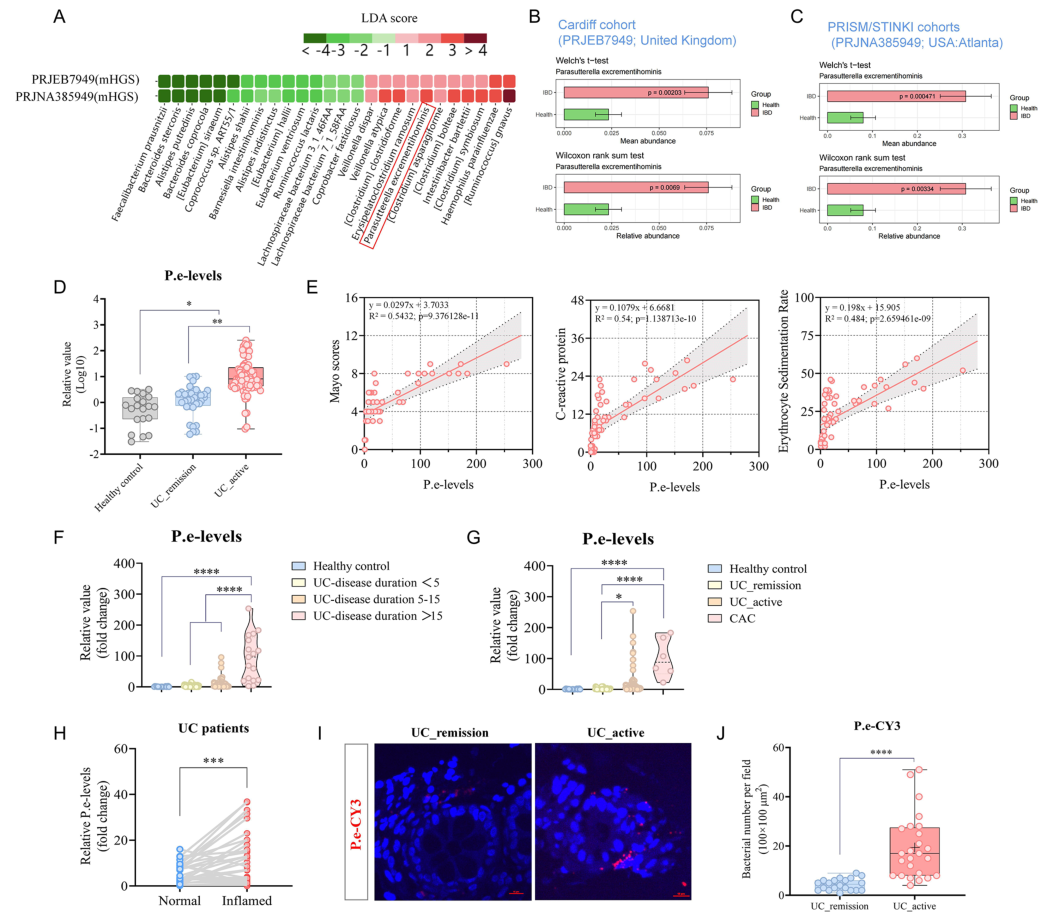
图2. UC患者中P. excrementihominis丰度升高
2、P. excrementihominis加剧小鼠结肠炎和CAC进展
为验证P. excrementihominis的致病性,构建了DSS诱导结肠炎和AOM/DSS诱导CAC小鼠模型,通过灌胃活细菌、热灭活细菌、细菌培养上清或对照培养基进行干预。结果显示,定植活P. excrementihominis的小鼠在DSS处理后,体重下降更显著、疾病活动指数(DAI)更高、结肠缩短更明显,组织学检查可见广泛上皮损伤和免疫细胞浸润;此外,细菌培养上清可完全复刻活细菌的致病效应,而热灭活细菌无此作用,提示其致病性依赖特定代谢产物。
免疫染色分析发现,P. excrementihominis主要诱导 Ly6G⁺中性粒细胞浸润至结肠固有层,而CD8⁺T 细胞、F4/80⁺单核巨噬细胞等其他免疫细胞的浸润在各组间无显著差异;通过Ly6G中和抗体耗竭中性粒细胞后,P. excrementihominis诱导的结肠炎症显著减轻,证实中性粒细胞是其致病的核心介质。在CAC模型中,P. excrementihominis或其培养上清均能显著增加结肠肿瘤的数量和体积,升高 Ki67⁺增殖细胞比例,同时促进NETs标志物(MPO、CitH3)及炎症因子(S100A8/9、MMP9)的表达;而Padi4敲除小鼠(NETs形成缺陷)中,P. excrementihominis诱导的结肠炎和CAC进展均得到显著缓解,进一步明确NETs在该细菌致病过程中的关键作用。
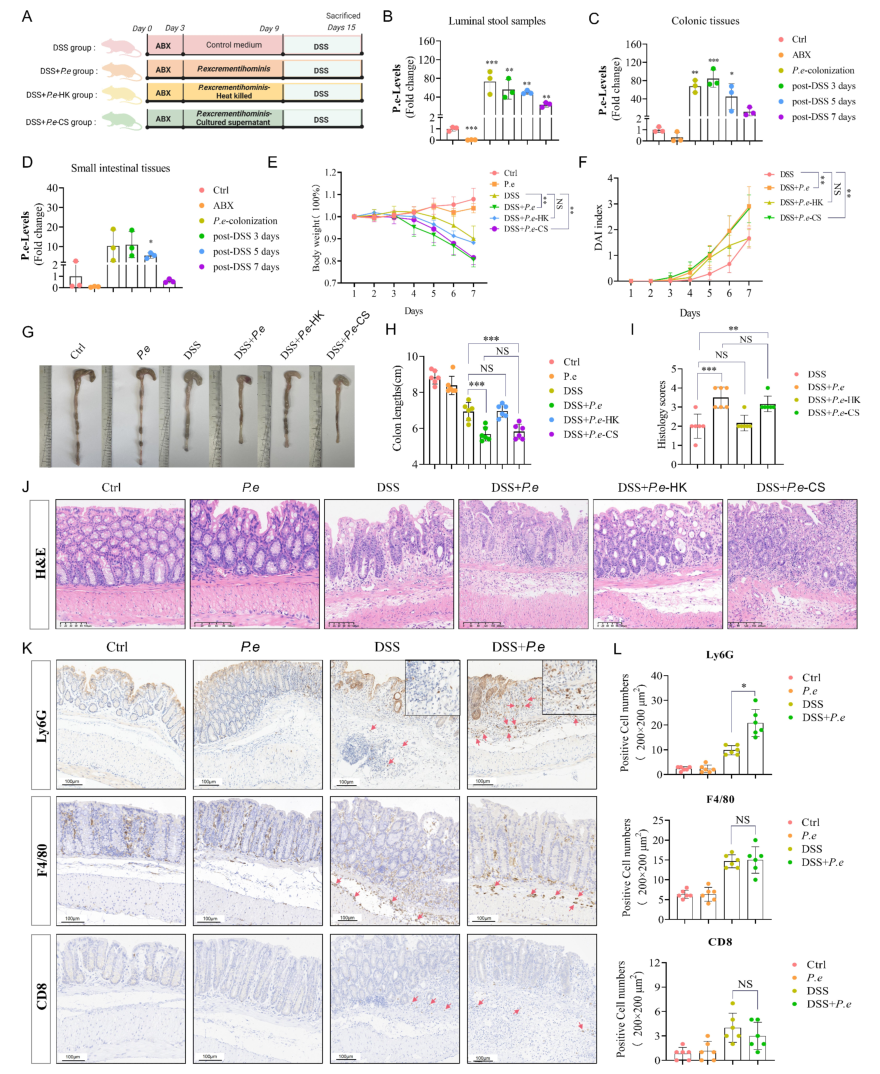
图3. P. excrementihominis加重小鼠结肠炎
3、P. excrementihominis通过代谢重编程产生关键致病代谢物
通过无菌小鼠单菌定植模型结合RNA测序和代谢组学分析,发现P. excrementihominis可显著重塑宿主代谢:RNA测序显示,定植小鼠结肠组织中碳水化合物代谢、脂解、淀粉蔗糖代谢相关基因显著上调,提示其增强宿主碳水化合物代谢能力;代谢组学进一步鉴定出,该细菌在体内(粪便、血清)和体外(培养上清)均能产生琥珀酸(Suc)和6-羟基己酸(6-HHA),且这两种代谢物在定植小鼠样本中丰度显著升高。
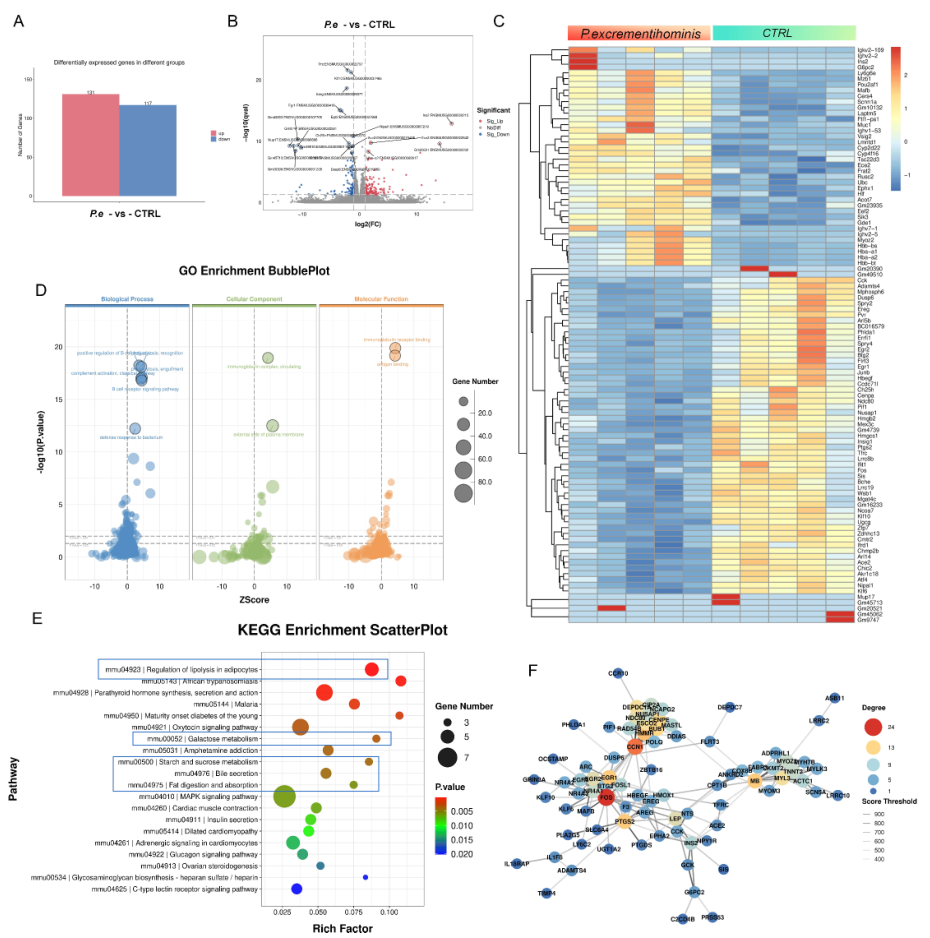
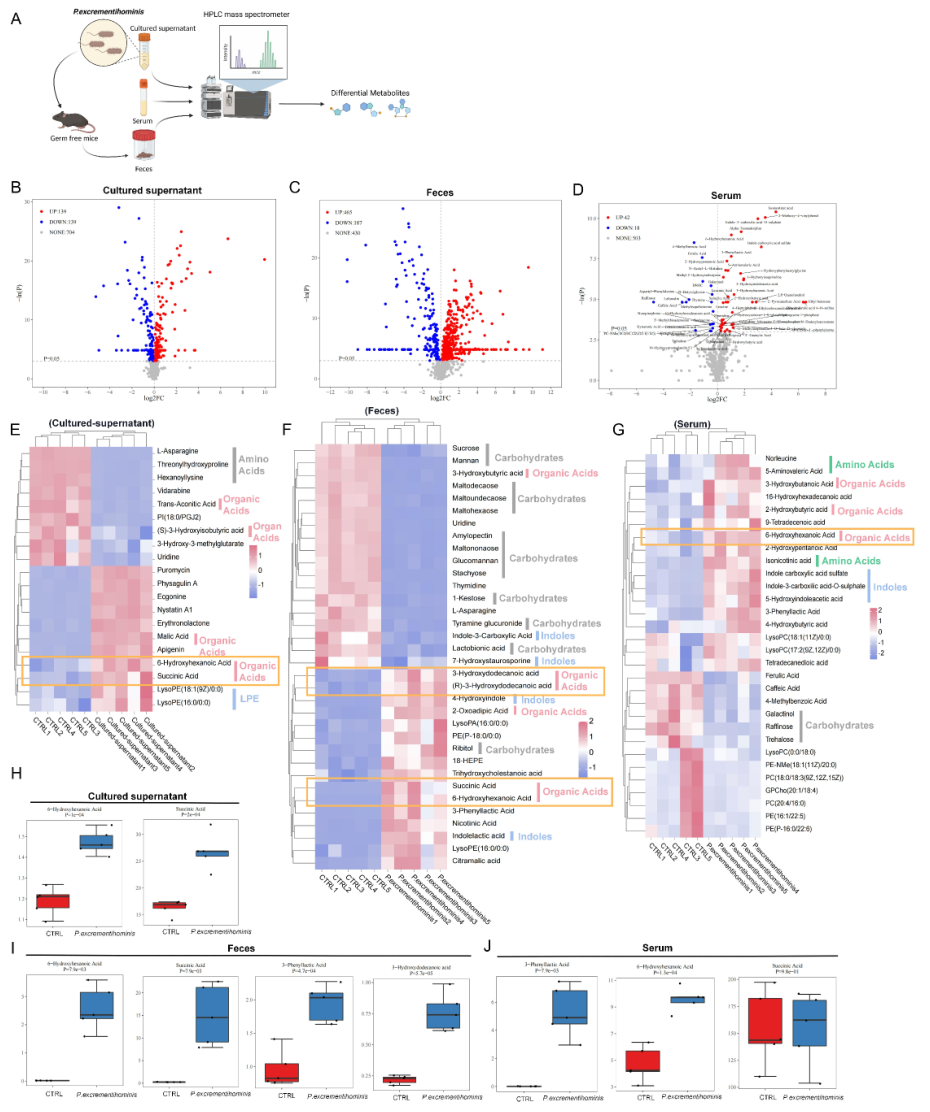
图4. P. excrementihominis重塑小鼠代谢谱,产生促炎代谢物
4、6-HHA和Suc通过SUCNR1/GPR84信号通路诱导GSDMD依赖的NETs
体外细胞实验发现,仅Suc和6-HHA能特异性增强LPS预处理的骨髓来源中性粒细胞和人多形核中性粒细胞中炎症介质(ELANE、S100A9、CCL4、IL-1β)和NETs相关基因(S100A8/9、MMP9/10、LCN2)的表达,促进MPO⁺/CitH3⁺ NETs形成及SYTOX Green阳性细胞数量增加;机制上,Suc可结合琥珀酸受体1(SUCNR1),6-HHA 可结合G蛋白偶联受体84(GPR84),二者共同激活NLRP3炎症小体和Gasdermin D(GSDMD)剪切,最终诱导GSDMD依赖的NETs形成。
体内验证显示,给DSS处理的野生型小鼠注射Suc和6-HHA,可显著加剧结肠炎症状(体重下降、粪便出血、结肠缩短)和组织损伤;在CAC模型中,这两种代谢物能显著增加肿瘤数量和大小,上调结肠组织中MPO、S100A8/9、剪切型GSDMD的蛋白表达。而中性粒细胞特异性GSDMD敲除小鼠(GSDMDfl/flS100A8-Cre)中,Suc和6-HHA诱导的CAC进展被完全阻断,肿瘤负担、炎症指标与对照组无显著差异,直接证实中性粒细胞GSDMD是代谢物诱导NETs形成及疾病进展的核心分子。
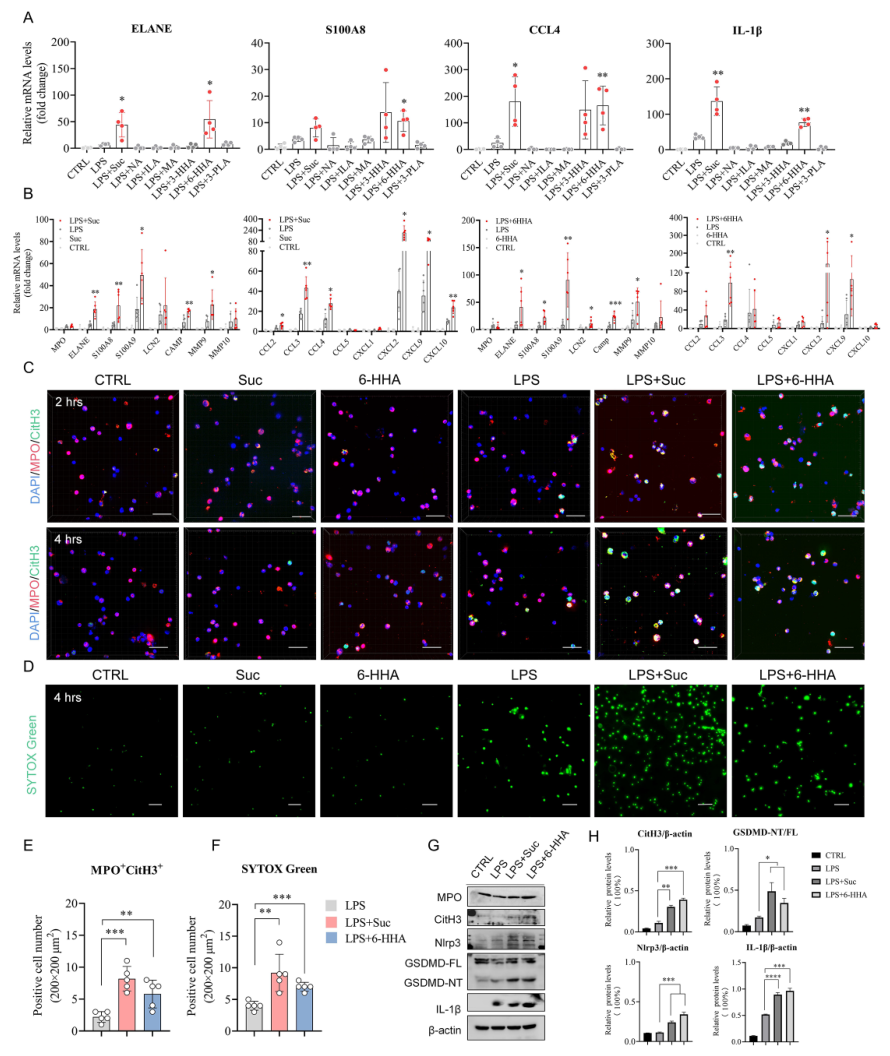
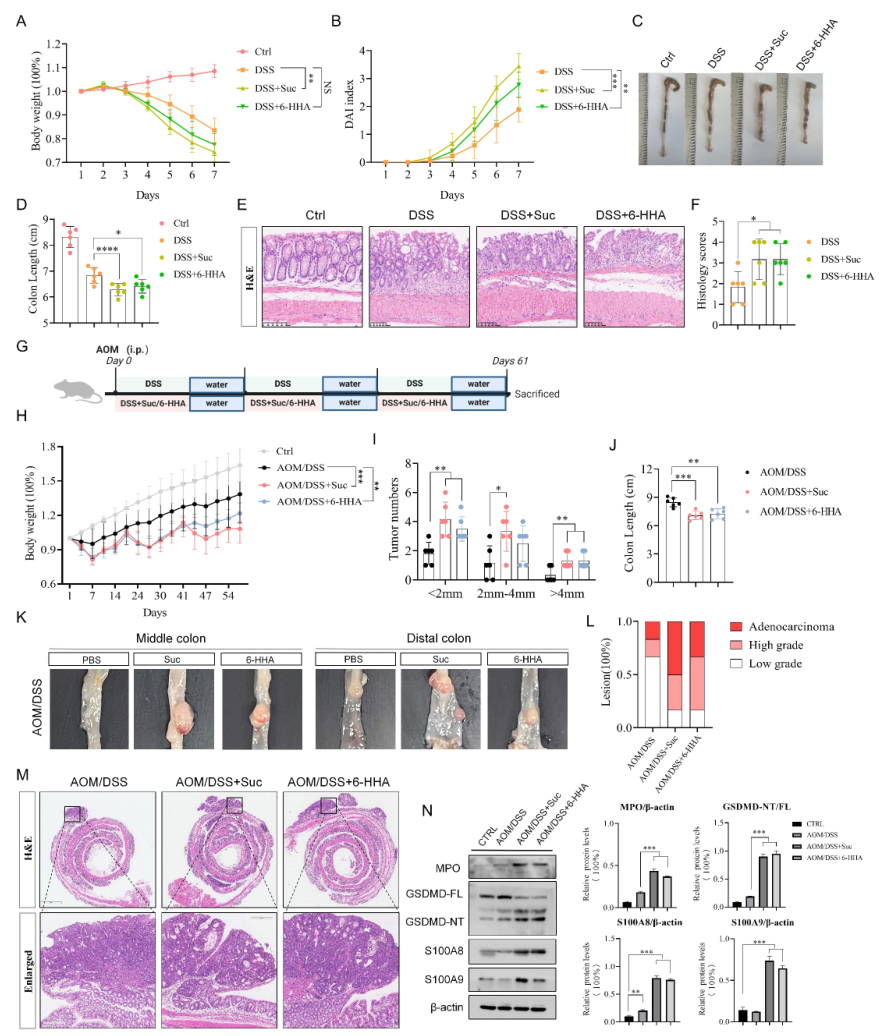
图5. 6-HHA和Suc促进GSDMD依赖性NETs
5、饮食与年龄对P. excrementihominis丰度的调控
16S rRNA测序分析显示,18月龄老年小鼠粪便中P. excrementihominis丰度显著高于2月龄年轻小鼠;粪便菌群移植(FMT)实验证实,将老年小鼠菌群移植给年轻小鼠后,受体小鼠的AOM/DSS诱导CAC表型显著加重,组织学检查进一步证实年龄相关的P. excrementihominis富集可加剧结肠肿瘤发生。
饮食干预实验显示,P. excrementihominis的丰度对饮食成分具有高度可塑性:高碳水化合物饮食、高脂饮食可显著促进其增殖,而生酮饮食(KTD)、高纤维饮食、低支链氨基酸饮食则能抑制其丰度,其中生酮饮食的抑制效果最为显著。
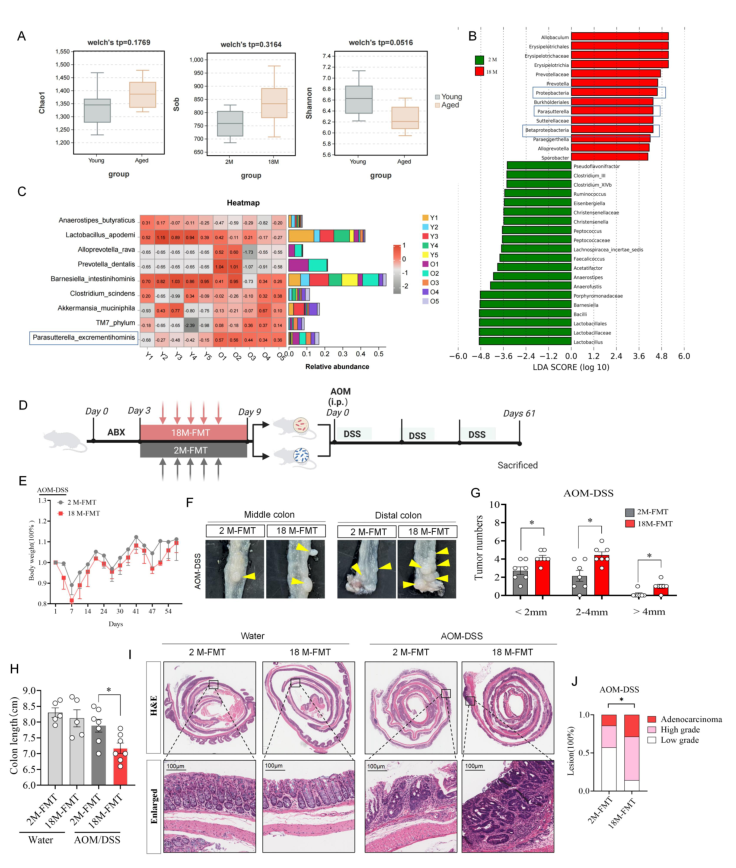
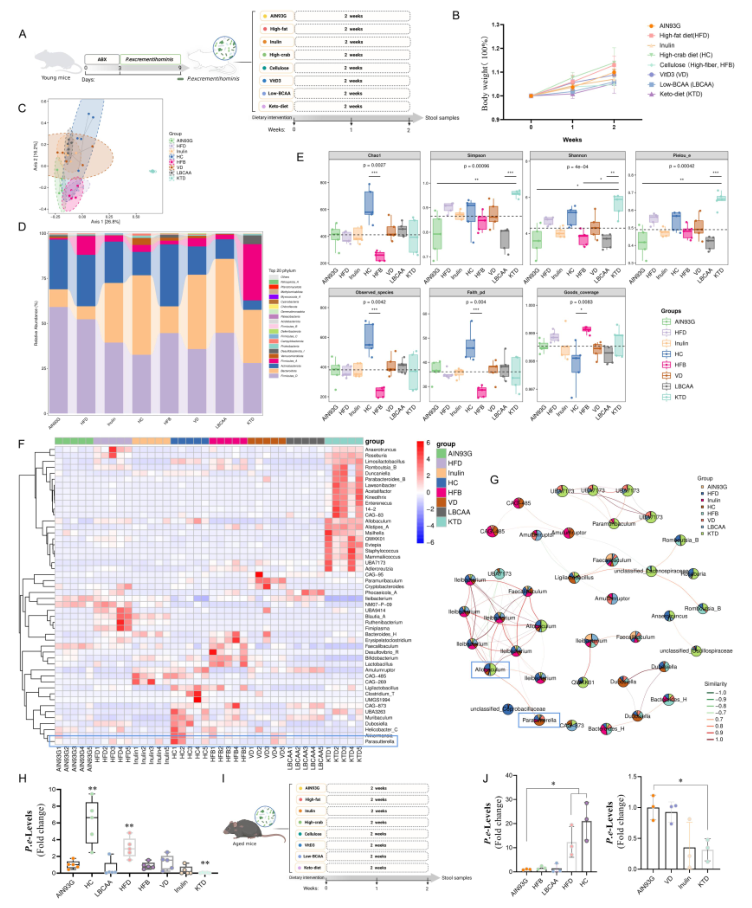
图6.饮食与年龄对P. excrementihominis丰度的调控
三、研究结论
本研究通过临床结合多组学研究探索并确认P. excrementihominis是溃疡性结肠炎UC和结肠炎相关结直肠癌CAC的关键致病微生物,其丰度与UC疾病活动度、持续时间及CAC风险正相关, 通过Suc和6-HHA两种关键代谢物,经SUCNR1/GPR84信号通路激活GSDMD依赖的NETs形成,进而加剧肠道慢性炎症和肿瘤发生。揭示 “细菌-代谢物-受体-NETs” 调控轴在UC和CAC中的作用,为UC和CAC提供新的治疗靶点。
参考文献
Parasutterella excrementihominis exacerbates experimental colitis and colitis-associated colorectal cancer via pathogenic NETosis activation. Gut. 2025
请扫描二维码阅读原文

绘谱帮你测
本研究发现Parasutterella excrementihominis 在UC及CAC患者粪便中显著富集,且其丰度与疾病活动度、病程及年龄密切相关,受高碳水饮食促进而生酮饮食抑制,通过麦特绘谱提供的非靶代谢组学进一步解析该细菌可通过增强宿主碳水化合物代谢产生琥珀酸(Suc)和6-羟基己酸(6-HHA),这两种核心代谢物是介导致病性 NETosis 的关键分子。
麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱已为数百家三甲医院、科研院所和企业提供多组学一站式整体解决方案,协助客户与合作伙伴发表SCI文章600+篇,累计影响因子6000+,平均IF>10,涵盖Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等顶级期刊。


