文献解读
Cell Metabolism | 贾伟等科学家揭秘“清醛益生菌”精准拦截高糖产乙醛通道,筑牢代谢防火墙
在全球范围内,代谢相关脂肪性肝病 (MASLD)已成为主要的慢性肝病。为什么有些人仅表现为单纯脂肪肝,而另一些人却迅速发展为严重的代谢相关脂肪性肝炎 (MASH)?
上海交通大学医学院附属第六人民医院转化医学中心/上海市糖尿病重点实验室贾伟教授、郑晓皎教授团队最新研究揭示了一项突破性机制:在高糖饮食的影响下,肠道菌群会产生乙醛,成为推倒健康多米诺骨牌的“幕后黑手”。这项研究不仅突破了肝病发病机制的认知界限,更通过合成生物学开发出“清醛益生菌”,为全球数亿肝病患者带来了全新的治疗希望。该研究于2026年3月3日在Cell Metabolism线上正式发表。

原文链接:https://www.cell.com/cell-metabolism/fulltext/S1550-4131(26)00043-4
嗜甜的代价
长期以来,果糖等高糖摄入一直被认为是脂肪肝的罪魁祸首。然而,糖分究竟如何引发类似酒精性肝炎的纤维化进程,悬而未解的谜题。针对这一疑问,研究团队通过对21万名患者的海量临床数据进行深入分析,明确揭示了高糖摄入与肝病死亡率之间的紧密关联(图1),为理解糖分在肝病发展中的关键作用提供了重要证据。
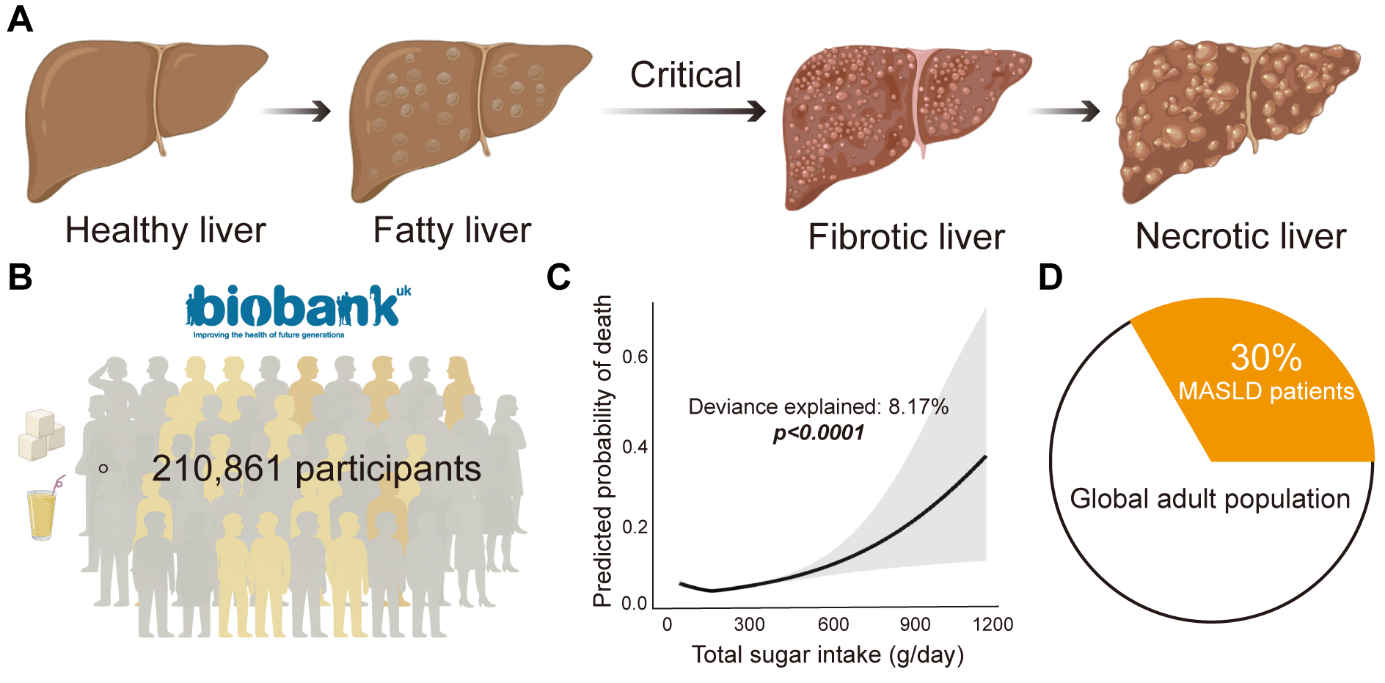
图1. 高糖摄入与肝病进展密切相关
更具突破性的是,糖分进入人体后,在失调的肠道菌群作用下被发酵产生高浓度的乙醛(图2)。这种无需饮酒便持续生成的酒精代谢毒素,悄然对肝脏造成致命打击,成为推动脂肪性肝炎(MASH)进展的隐形杀手。
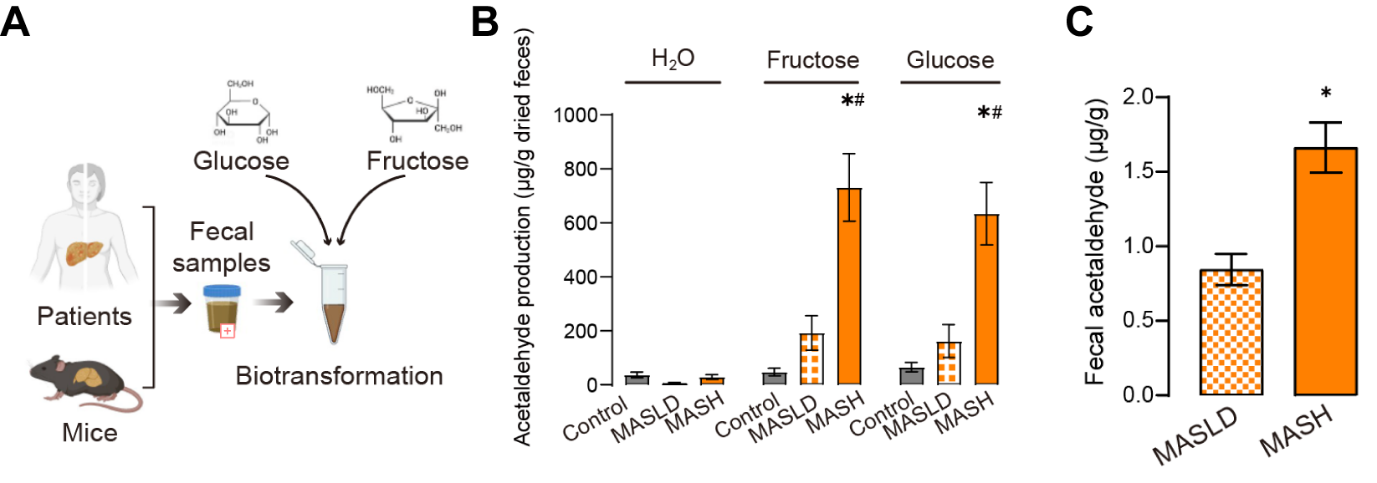
图2. 临床MASH患者的粪便乙醛转化能力
机制创新
研究团队深入揭示:肠源性乙醛通过门静脉直接输送到肝脏,精准开启基质金属蛋白酶7(MMP7)的表达。MMP7的激活不仅破坏了肝脏细胞外基质的正常平衡,更引发了胶原蛋白的级联沉积,推动纤维化的发生。这一发现,将对MASH的研究视角从宏观的代谢紊乱,升华到分子层面上的基质重塑,为早期干预提供了极具潜力的全新靶点(图3),为肝纤维化的治疗开辟了崭新的科研路径。
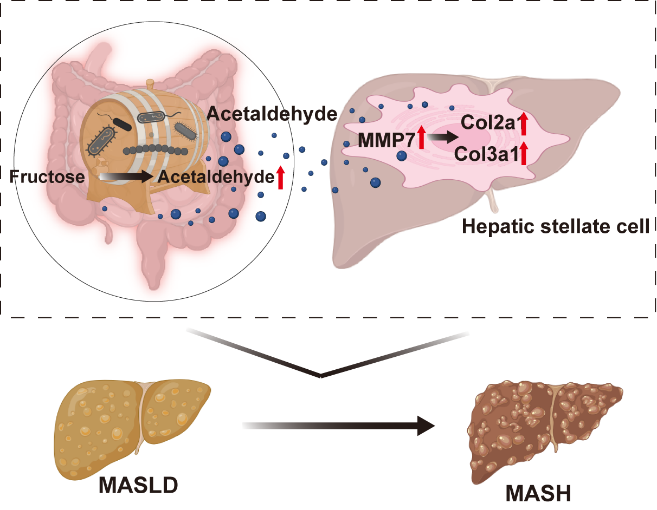
图3. 内源性乙醛促进MASH进展的分子机制
打造“靶向清醛”益生菌
科研的最终目标是治病救人。贾伟和郑晓皎团队不仅在机制研究方面取得了突破,更展现了前瞻性的转化医学视野:既然内源性乙醛源自肠道,何不在其进入肝脏之前予以就地根除?秉持源头治理的理念,团队从“饮酒不伤肝”人群中筛选出具备天然清除乙醛能力的益生菌菌株(Ligilactobacillus salivarius CTMT1),并借助合成生物学技术对其进行工程化改造,研发出过表达乙醛脱氢酶的工程菌株HAM(Ligilactobacillus salivarius CTMT2)。这两款靶向“清醛益生菌”,能够在肠道内精准捕获并高效降解乙醛,构建一道严密的代谢防火墙,有效阻挡肠源乙醛进入肝脏。
在多项临床前动物模型中,天然益生菌和工程菌株HAM不仅显著降低了肝脏内的乙醛浓度和转氨酶水平,减少了肝脏炎症反应,更展现出逆转已形成肝脏纤维化的巨大潜力(图4)。此外,这些菌株具有极高的生物安全性,为满足全球范围内MASH的临床迫切需求,提供了基于肠道微生态调控的创新治疗范式。这一突破标志着代谢性肝病的预防和治疗正式迈入以精准、低毒、源头干预为核心的新时代,为肝病防治开辟了崭新路径。
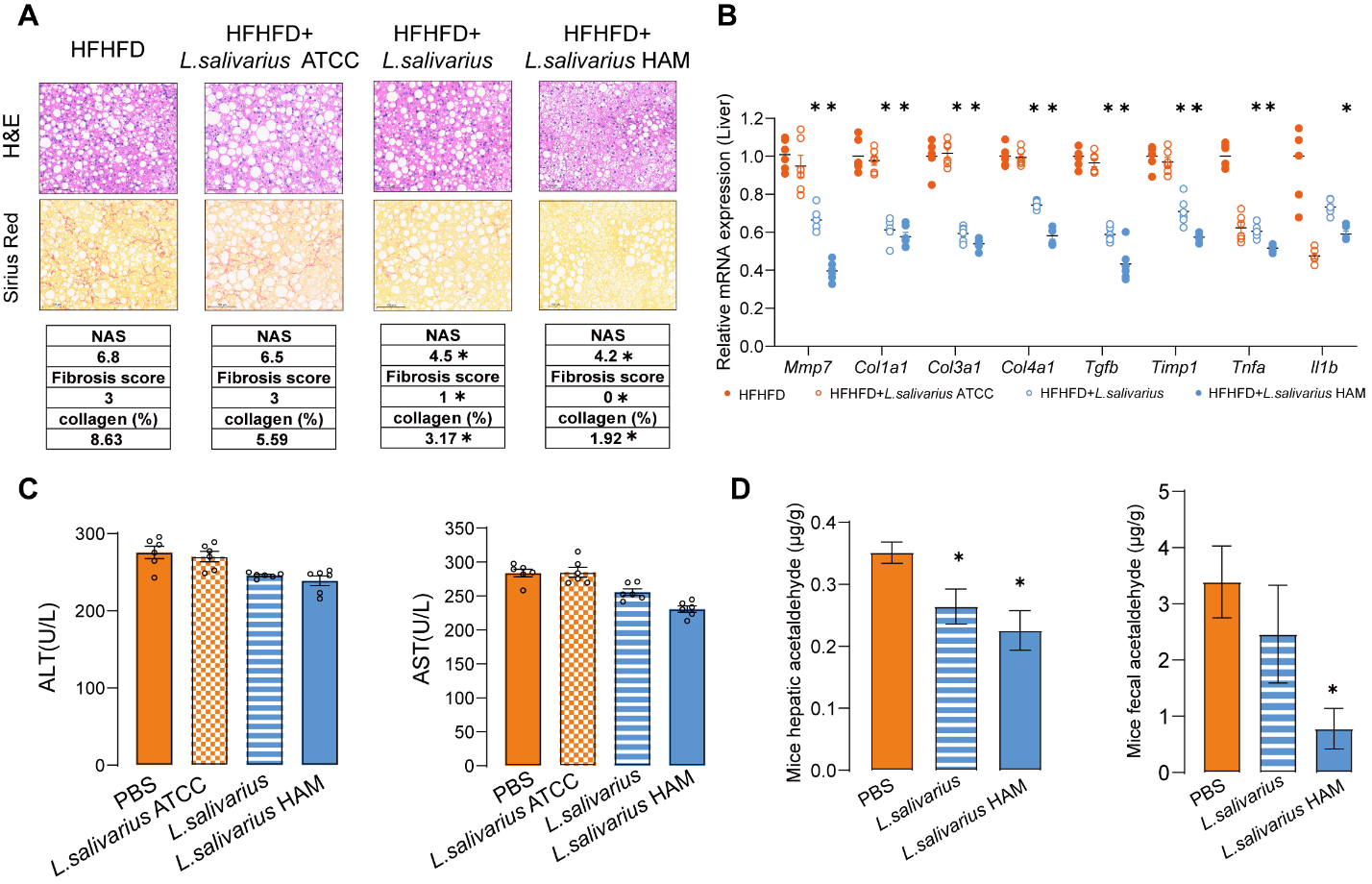
图4. 益生菌缓解MASH模型小鼠代谢表型
“清醛菌”的五大优势
01、源头阻断
传统药物多聚焦于肝脏治疗,作用于已发生的损伤。而“清醛菌”在肠道内建立天然的乙醛降解屏障,实现了“肝病肠治”的源头干预和精准代谢调控,从根本上阻断有害物质的肝脏积累。
02、广泛的适应症范围
针对高糖饮食引发的非酒精性脂肪肝,“清醛菌”能精准清除内源性乙醛,逆转肝脏代谢应激,改善脂肪堆积;面向ALDH2缺陷(如东亚“脸红”人群),加速肠道乙醛降解,缓解饮酒后不适,降低急性中毒风险;针对长期酗酒导致的酒精性肝病,“清醛菌”有效抵御乙醛引发的多系统损伤,为慢性肝损提供持续修复。
03、机制的安全性
“清醛菌”源自人体健康微生态,具有良好的生物相容性。主要作用于肠腔,不进入血液循环,从而大大降低化学药物常见的肝肾毒性及全身代谢负担,安全性极高。
04、成本与便利性
通过发酵工艺,“清醛菌”制剂可实现大规模生产,成本远低于传统药物。同时,采用口服给药方式,极大提升慢性肝病患者的依从性,适合广泛推广,满足脂肪肝等慢性疾病的持续管理需求。
05、多效保护与协同
除了高效降解乙醛,“清醛菌”还能改善肠道微生态屏障,减少脂多糖等有害物质的易位,带来系统性的健康益处。这种多重保护作用远超单一化学药物的效果,为肝脏疾病的综合治疗提供了全新思路(图5)。
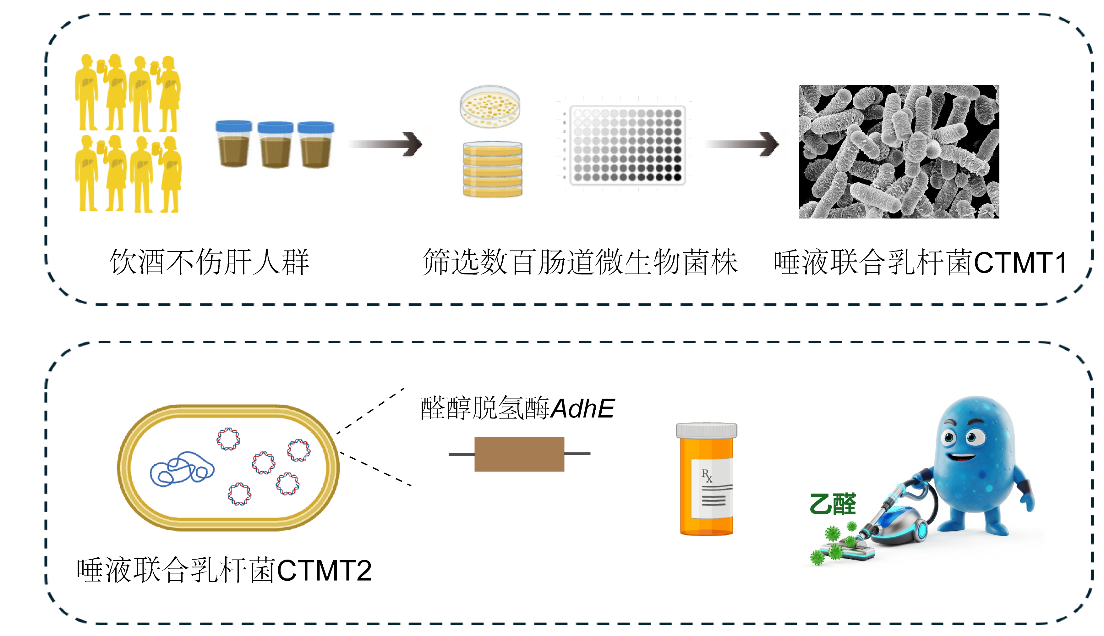
图5. 新型“清醛菌”研发思路
延伸阅读
围绕肠-肝轴调控代谢相关脂肪性肝病的深层作用机制,贾伟教授与郑晓皎教授,联合贾伟平院士团队,于2023年在国际顶刊Cell Metabolism发表重要研究成果,立足肠-肝轴调控网络,首次揭示猪去氧胆酸缓解非酒精性脂肪性肝病的新机制——通过调节肠道微生态与肝脏代谢稳态,改善肝脏脂质沉积,为脂肪肝的防治提供了关键靶点与干预策略。(点击查看文章)
• 本研究由上海交通大学医学院附属第六人民医院贾伟教授和郑晓皎教授作为共同通讯作者完成。
• 上海交通大学医学院附属第六人民医院唐雅珺副研究员和况俊良助理研究员为本文共同第一作者。
• 该研究获得了国家科技部重大项目、国家自然科学基金、国家重点研发计划、上海市自然科学基金等项目的资助。
麦特绘谱创始人贾伟教授十年深耕肝病领域研究
贾伟教授团队长期深耕肠-肝轴、胆汁酸代谢与肠道菌群领域,围绕肝病、代谢性疾病及神经退行性疾病的发病机制与干预策略展开系统性研究,推动了肠-肝轴领域从基础研究向临床转化的跨越。
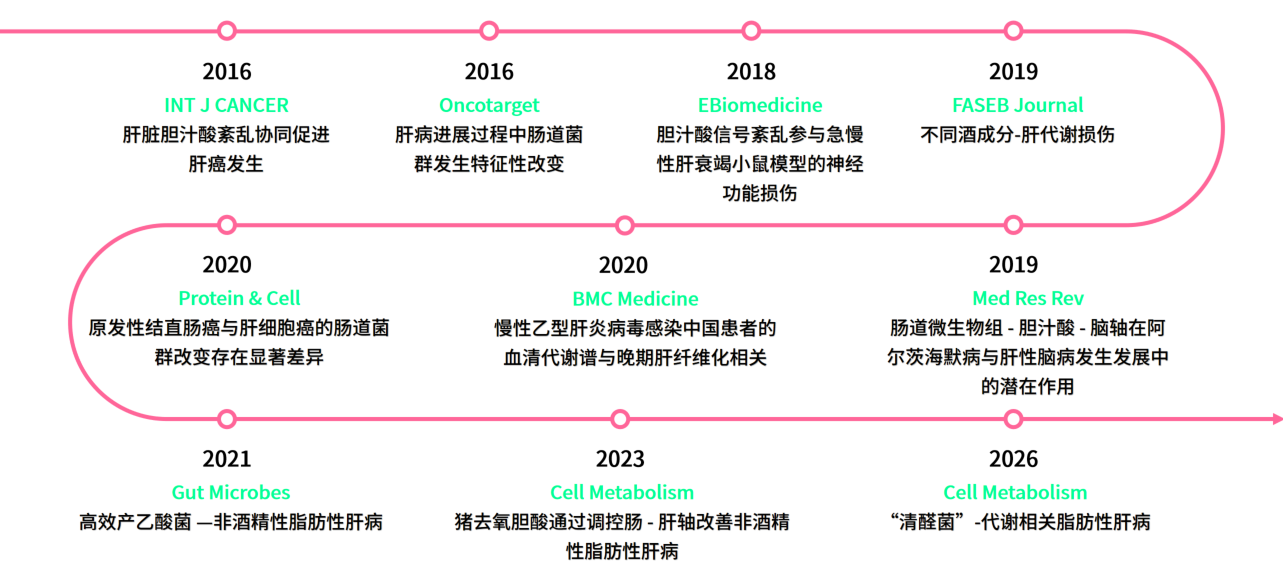
麦特绘谱护航顶刊研究
麦特绘谱依托贾伟教授团队的前沿科研积累,构建Q200、Q300、Q500、Q1000、QL1000和胆汁酸、短链脂肪酸、色氨酸及吲哚衍生物、多胺和TMAO类等各类小分子代谢物、非靶向代谢组学和同位素示踪代谢流技术等共40+系列检测方法,为全球科研与临床客户提供精准、高效的多组学解决方案。
凭借稳定、精准、高覆盖的技术优势,麦特绘谱已持续助力国内外科研团队在Cell Metabolism, Gut, Nature Metabolism, Cell Host & Microbe等肝病领域发表高分论文数百篇。从机制发现到靶点验证,从基础研究到临床转化,麦特绘谱将继续以精准代谢组学为引擎,推动疾病早筛、机制研究与创新疗法不断突破,为守护国人健康持续贡献力量。



