文献解读
客户案例 | Gut:幽门螺杆菌不再是唯一!房静远院士团队揭示胃癌又一“促癌元凶”咽峡炎链球菌
胃癌(GC)的发病率和死亡率位居全球恶性肿瘤前五,东亚地区尤为高发,是我国癌症相关死亡的主要原因之一。长期以来,幽门螺杆菌(H. pylori)被公认为胃癌发生的核心风险因素,但非幽门螺杆菌肠道菌群在胃癌发生发展中的作用仍未明确。前期有研究证实,咽峡炎链球菌(S. anginosus)是胃癌筛查的非侵入性敏感生物标志物,其表面蛋白TMPC可通过介导细菌黏附与定植促进小鼠胃癌发生,但该菌与宿主的代谢相互作用等其他致病途径尚未被揭示。
2026年1月,上海交通大学医学院附属仁济医院房静远院士团队在Gut上在线发表了题为“Streptococcus anginosus-derived methionine promotes gastric cancer progression”的研究文章,通过临床队列发现→多组学分析→机制验证→临床菌株确认的闭环研究设计,揭示了咽峡炎链球菌通过metE基因依赖的甲硫氨酸生物合成途径,分泌甲硫氨酸激活宿主甲硫氨酸循环,从而促进胃癌细胞增殖和肿瘤进展。(麦特绘谱提供一碳代谢技术检测服务)
【研究设计】

图1. 技术路线
【研究结果】
1.S. anginosus在胃癌患者中富集且具有明确促癌效应
通过对212份粪便样本宏基因组测序分析,研究首先证实:胃癌患者粪便中S. anginosus的丰度与检出率均显著高于慢性胃炎患者,且这一富集现象不受H. pylori感染状态、年龄、性别及BMI等混杂因素影响,提示其与胃癌的关联具有独立性。
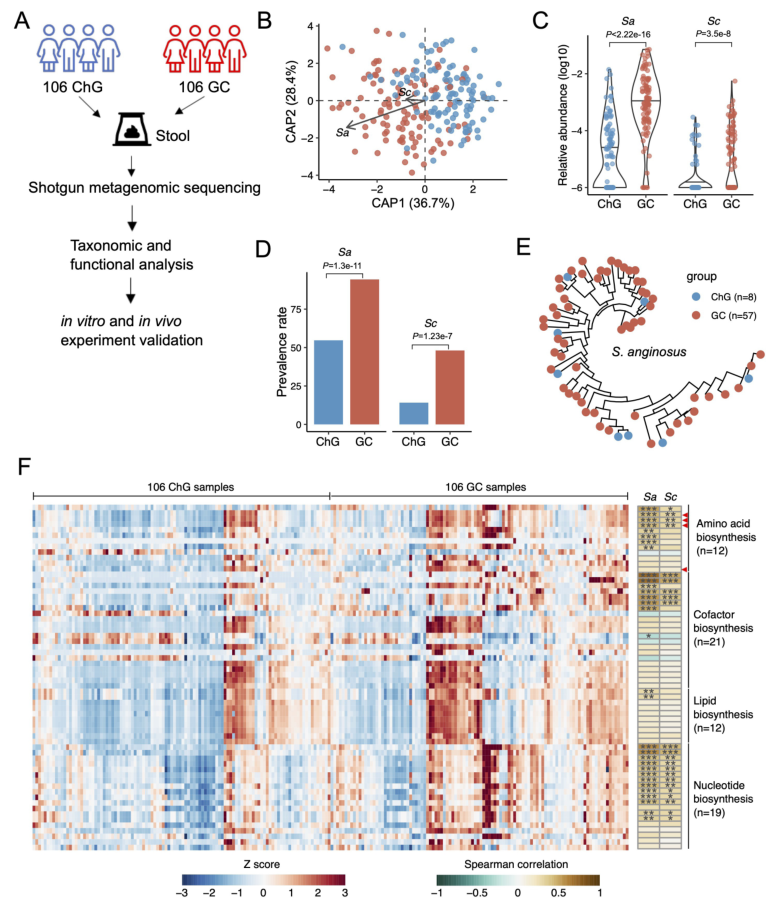
图2. S. anginosus在胃癌患者中富集
体外细胞实验进一步验证了其促癌活性:S. anginosus以剂量依赖方式促进 胃癌细胞(AGS、HGC27、MGC803 )增殖,不仅提升 EdU 阳性细胞比例(增殖标志物),还显著增加集落形成的数量与大小;而热灭活处理后的S. anginosus完全丧失了这一促增殖效应,提示其促癌作用依赖细菌的活性状态。
体内实验中,BALB/c裸鼠异种移植模型显示,S. anginosus处理组肿瘤重量和体积显著大于对照组,Ki-67增殖指数升高;ApcMin/+小鼠原位肿瘤模型中,S. anginosus处理组肿瘤发生率同样增加。
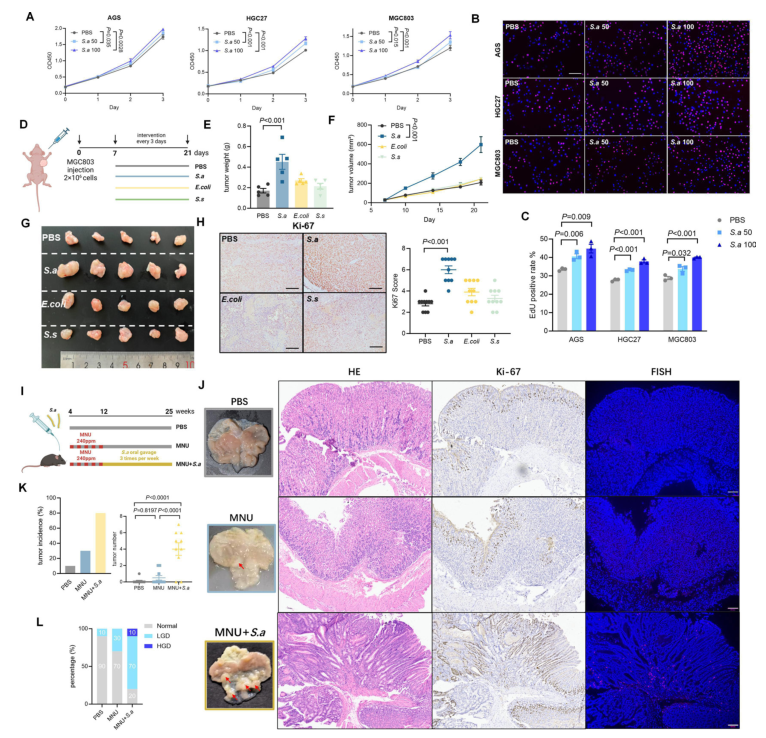
图3. S. anginosus具有促癌效应
2. 甲硫氨酸是S. anginosus促癌的核心代谢产物
宏基因组功能富集分析进一步发现,在胃癌患者粪便中4条甲硫氨酸生物合成通路(HOMOSER-METSYN-PWY等)显著富集,且与S. anginosus丰度呈正相关。
靶向代谢组学结果证实,胃癌组织中半胱氨酸-甲硫氨酸代谢通路是差异最显著的通路,且S. anginosus丰度与甲硫氨酸水平呈正相关;体外培养实验显示,S. anginosus培养上清液的甲硫氨酸水平显著高于大肠杆菌和唾液链球菌,证实S. anginosus具备高效合成甲硫氨酸的能力;S. anginosus处理组小鼠的胃黏膜和肿瘤组织中,甲硫氨酸水平显著升高;而青霉素(对S. anginosus敏感)干预或甲硫氨酸限制饮食,不仅能降低甲硫氨酸水平,还能同步逆转S. anginosus的促肿瘤生长效应,证实甲硫氨酸是介导这一病理过程的关键代谢介质。
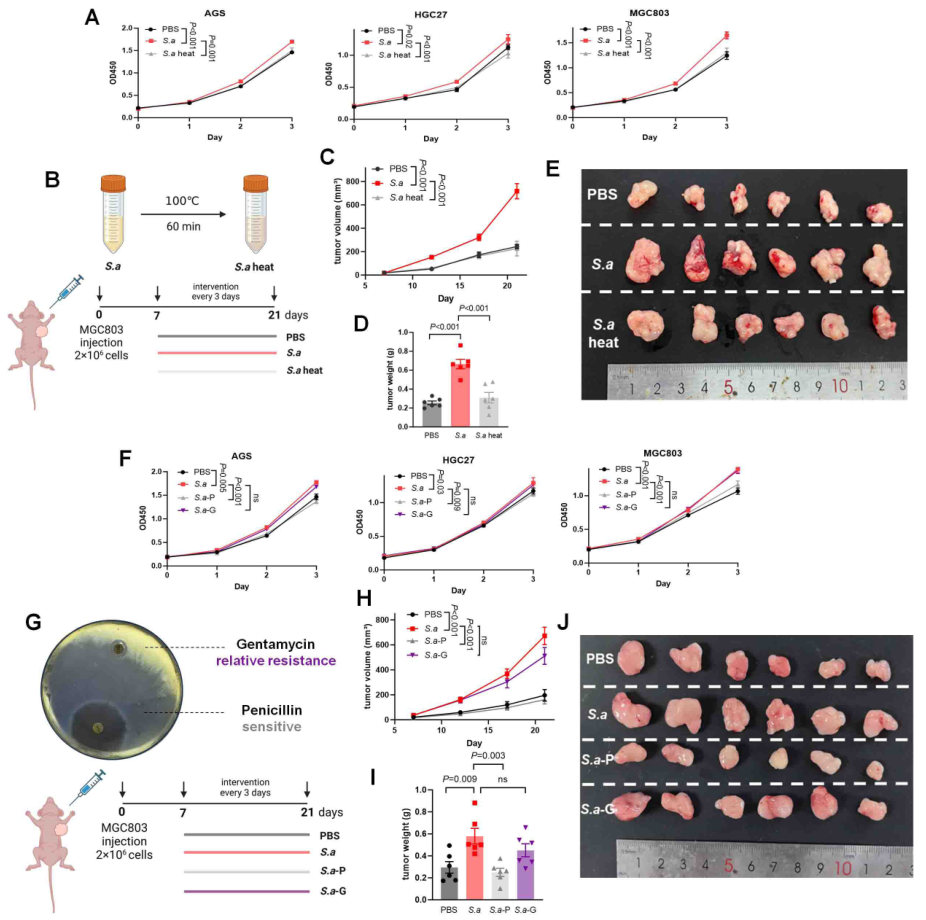
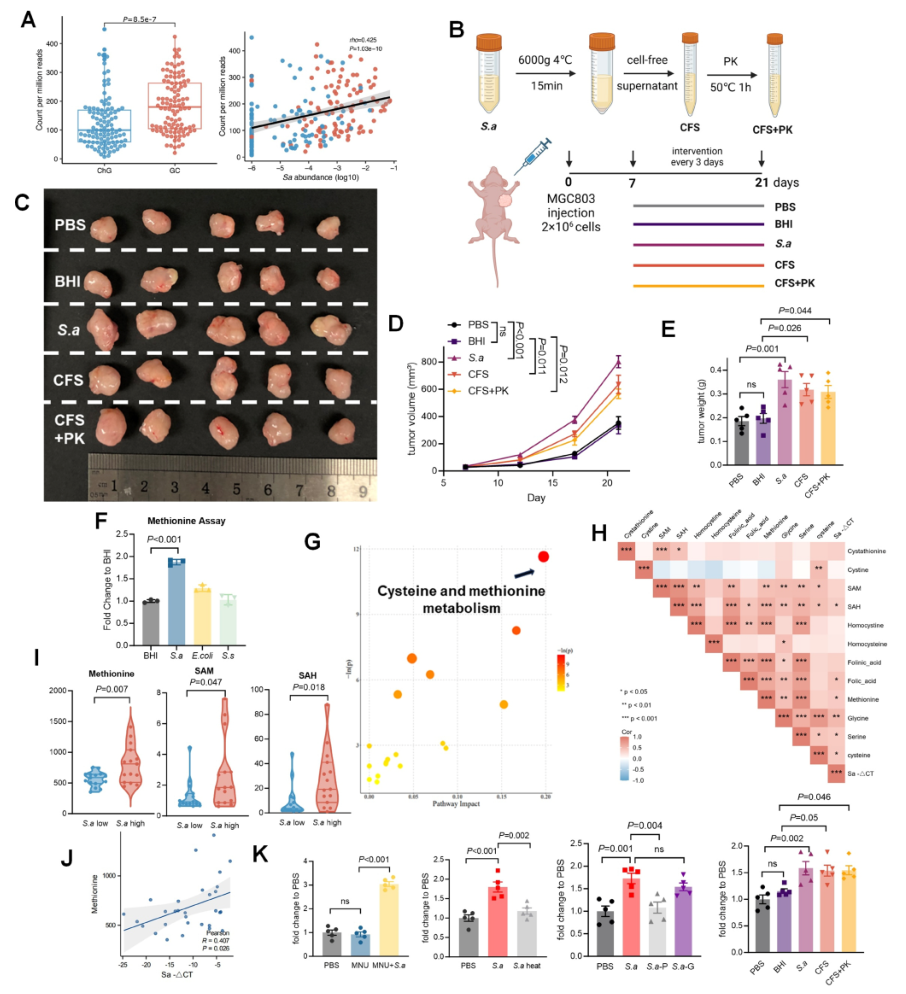
图4. 甲硫氨酸是S. anginosus促癌的核心代谢产物
3. metE基因是S. anginosus合成甲硫氨酸的关键
为解析S. anginosus合成甲硫氨酸的分子机制,研究对甲硫氨酸合成通路的核心基因(metA、metB、metC、metE)进行了系统分析:宏基因组数据显示,metB、metC、metE在胃癌样本中的丰度显著高于慢性胃炎样本,其中metE的丰度最高且在不同来源的S. anginosus菌株中高度保守。
为验证metE的功能,研究构建了S. anginosus ΔmetE突变株:与野生型菌株相比,突变株的培养上清液中甲硫氨酸水平显著下降,且无法促进胃癌细胞增殖;同位素标记实验进一步证实,S. anginosus可通过metE介导甲硫氨酸合成,敲除 metE后,m+4甲硫氨酸的生成量明显减少。体内实验同样显示,ΔmetE突变株处理组的肿瘤生长速度、重量均显著低于野生型组,且胃组织中甲硫氨酸水平无明显升高,明确了metE基因在甲硫氨酸合成及促癌效应中的核心作用。
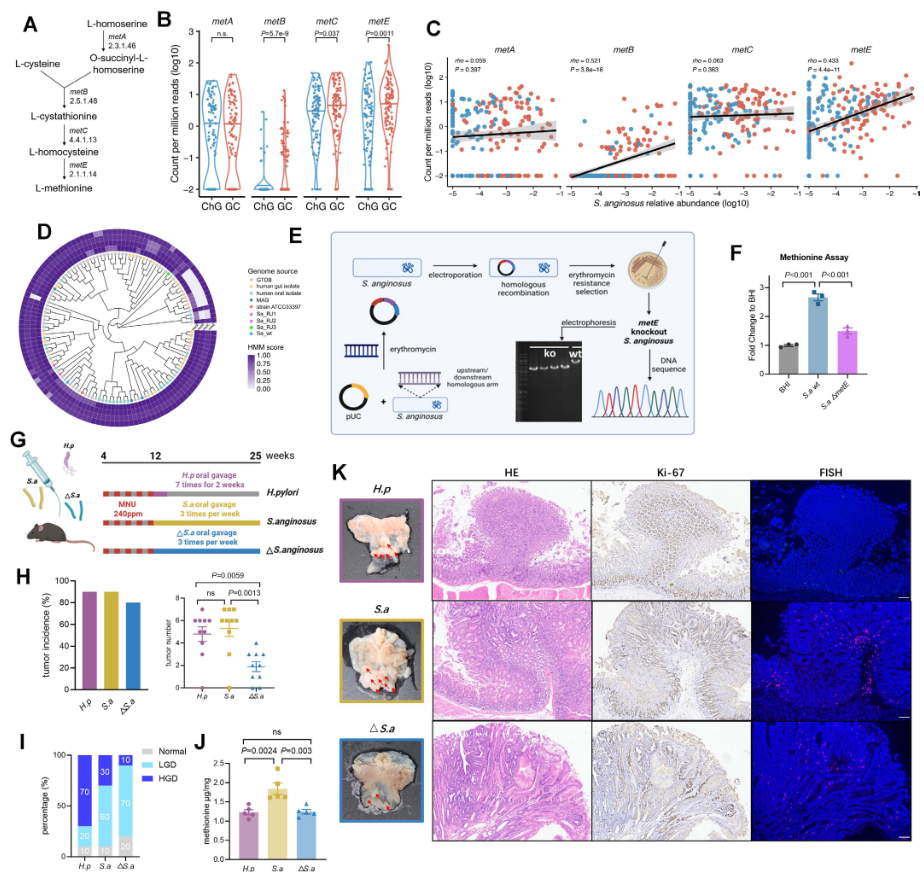
图5.metE基因敲除逆转S. anginosus的促癌作用
4. 临床分离菌株验证促癌机制
为进一步研究其临床转化价值,从30例胃癌患者的癌组织中,成功分离培养出3株S. anginosus临床菌株(RJ1、RJ2、RJ3),全基因组测序显示,这些临床菌株与参考菌株的平均核苷酸一致性(ANI)>95%,且均携带metE及其他甲硫氨酸合成相关基因。
体内功能验证显示,3株临床分离菌株均能显著促进裸鼠异种移植肿瘤的生长,其培养上清液中的甲硫氨酸水平与野生型菌株相当;肿瘤组织检测结果显示,临床菌株处理组的Ki-67增殖指数及甲硫氨酸、S-腺苷甲硫氨酸(SAM)、S-腺苷高半胱氨酸(SAH)等代谢物水平均显著升高,与野生型S. anginosus的作用完全一致,直接证实临床胃癌组织中的S. anginosus确实能通过合成甲硫氨酸推动肿瘤进展。
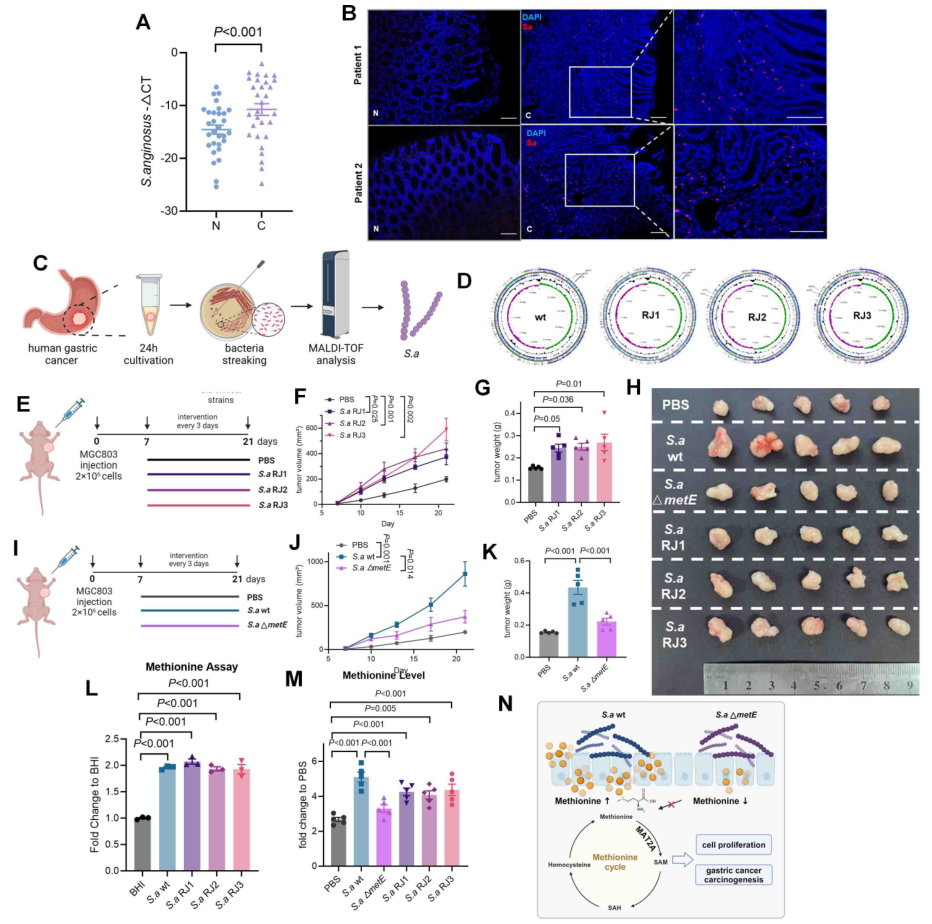
图6. S. anginosus的临床分离菌株及其促癌作用
研究结论
本研究通过 “临床队列-组学发现-体外验证-体内建模-临床菌株分离” 的系统性研究,首次明确了咽峡炎链球菌(S. anginosus)促进胃癌进展的新型代谢机制:S. anginosus在胃癌患者体内特异性富集后,通过其保守的metE基因介导甲硫氨酸合成,该代谢产物进入肿瘤微环境后,激活宿主细胞的甲硫氨酸循环,进而促进癌细胞增殖和肿瘤进展,揭示了 “细菌-代谢产物-宿主代谢重编程” 的致病通路,为胃癌的防控与治疗提供了新的靶点和线索。
参考文献
Streptococcus anginosusderived methionine promotes gastric cancer progression. Gut. 2026
请扫描二维码阅读原文

绘谱帮你测
本研究中通过对一碳代谢通路中甲硫氨酸等关键代谢物进行测定(麦特绘谱提供一碳代谢技术检测服务),为S. anginosus富集与甲硫氨酸代谢通路激活的关联提供了直接代谢证据,阐述了“细菌-代谢物-宿主代谢重编程” 这一核心致病机制。麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱已为数百家三甲医院、科研院所和企业提供多组学一站式整体解决方案,协助客户与合作伙伴发表SCI文章600+篇,累计影响因子6000+,平均IF>10,涵盖Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等顶级期刊。


