文献解读
绘谱导读 | 藏在代谢稳态里的健康新认知:饮食模式、犬尿氨酸通路和肠菌代谢产物
导读聚焦
代谢是生命活动的核心纽带,串联起营养摄入、细胞功能、疾病发生与免疫调控的全过程,其细微紊乱都可能引发全身连锁反应。
本期绘谱导读汇总近期高影响力研究,涵盖肝癌、胃癌、卒中、代谢性肝病等多种疾病,聚焦慢性应激、饮食模式、肠道菌群代谢等关键调控因素,解析烟酸、犬尿氨酸-犬尿喹啉酸代谢、NAD代谢重编程、牛磺酸转运、肠菌丁酸代谢转化、脂质重塑等核心机制,探讨饮食代谢干预、益生菌应用的潜在价值,同时挖掘肿瘤免疫治疗的新靶点。
这些研究打破传统认知,为疾病预防、临床诊疗提供了全新思路,也让我们对代谢稳态的重要性有了更深刻的认知。
导读目录
- Nature Metabolism | 慢性应激通过重塑犬尿氨酸代谢,削弱免疫细胞监视,从而导致肝癌
- Nat Commun | 高碳/脂比饮食可引发不利的代谢改变,该效应与体重无关
- Journal of Hepatology | 生酮与非生酮减重饮食对MASLD肝脏脂肪变性和线粒体代谢的不同影响
- Nature Comunications | SLC6A6将牛磺酸转运至线粒体以维持线粒体翻译和肿瘤生长
- GUT | 揭示人类肠道菌Dysosmobacter welbionis将肌醇转化为丁酸盐的独特途径及其益生菌潜力
- GUT | A. baumannii通过烟酸介导的NAD代谢重编程和糖酵解激活促进胃癌转移
- GUT | 犬尿喹啉酸通过肠脑神经环路减轻卒中后的脑损伤
- Cell Metabolism | 微生物代谢产物 FAD 能促使脂肪细胞进行脂质重塑,提升癌症免疫治疗效果
资源领取
本期导读文献原文,请在公众号后台回复“2026年2月绘谱导读”,即可获取资源链接。
01、Nature Metabolism | 慢性应激通过破坏肝脏犬尿氨酸代谢并削弱免疫监视促进肝癌进展

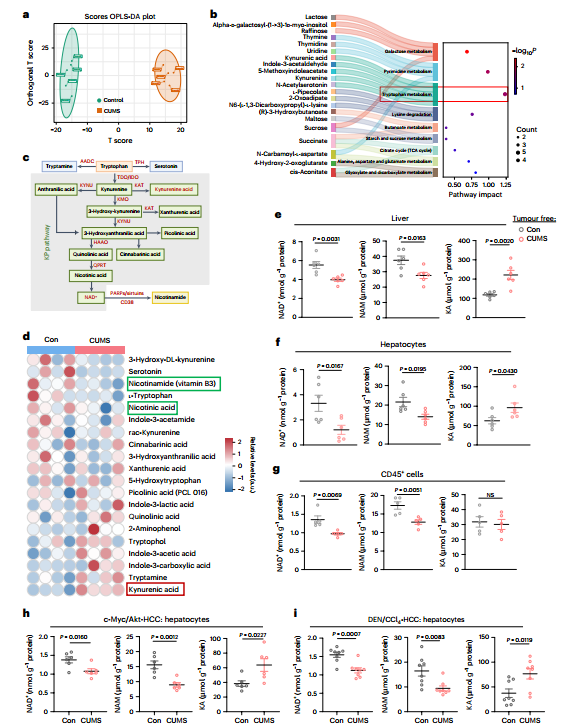
心理压力与肝脏疾病密切相关,但其潜在机制尚不明确。本研究揭示了一条脑-肝调控轴:慢性压力通过破坏儿茶酚胺/β2-肾上腺素能受体信号,抑制肝细胞中磷酸核糖转移酶表达,导致犬尿氨酸代谢从合成烟酰胺腺嘌呤二核苷酸转向犬尿喹啉酸积累,进而诱导线粒体功能障碍和肝脏CD8+ T细胞免疫监视受损,加速肝癌进展。
1、首先通过动物模型,发现在多种肝癌模型中慢性应激小鼠肿瘤负荷显著增加,流式细胞术分析显示,应激小鼠肝癌组织中CD8+T细胞数量显著减少,凋亡增加、活化标志物下调、耗竭标志物上调、效应分子表达减少。随后通过代谢组学技术,发现慢性应激小鼠肝脏组织中犬尿氨酸代谢失衡最为突出。ELISA检测显示,应激小鼠肝细胞中烟酰胺腺嘌呤二核苷酸和烟酰胺水平显著降低,而犬尿喹啉酸水平升高。
2、单细胞RNA-seq数据显示,β2-肾上腺素能受体是肝细胞中最丰富的肾上腺素受体,且在应激小鼠中表达下调。利用肝细胞特异性Adrb2敲除小鼠,证实Adrb2缺失可模拟慢性应激表型,导致肝细胞烟酰胺腺嘌呤二核苷酸减少、犬尿喹啉酸增加,以及CD8+ T细胞数量减少和功能受损。通过AAV病毒在肝细胞中过表达Adrb2可逆转慢性应激的上述效应。
3、通过RT-qPCR筛选发现,慢性应激小鼠肝细胞中犬尿氨酸通路关键酶Qprt表达显著下调。机制研究表明,ADRB2通过cAMP-CREB信号通路调控QPRT表达。染色质免疫沉淀证实CREB可直接结合于Qprt启动子区域。过表达Qprt在体内外均能逆转Adrb2缺失或慢性应激诱导的犬尿氨酸代谢失衡,恢复CD8+T细胞数量和功能,抑制肝癌进展。
4、通过RNA-seq和代谢分析发现,慢性应激小鼠肝脏CD8+T细胞出现明显线粒体功能障碍,基础呼吸、最大呼吸和ATP产生减少。烟酰胺和AHR抑制剂处理可恢复线粒体功能,而线粒体复合物I抑制剂鱼藤酮可消除肝细胞Adrb2缺失对CD8+T细胞的影响。
5、最后在临床转化方面,通过TCGA数据库和34例肝癌患者样本证实,肝细胞ADRB2和QPRT表达与烟酰胺腺嘌呤二核苷酸水平及CD8+T细胞功能呈正相关,与犬尿喹啉酸水平和CD8+T细胞凋亡呈负相关。利用人肝脏类器官模型证实,过表达ADRB2或QPRT可改善共培养CD8+T细胞的线粒体功能和效应分子表达。
参考文献:Sun R, Jiao D, Yuan W, et al. Chronic stress drives liver cancer by impairing the hepatic kynurenine pathway and immune surveillance. Nat Metab. 2026.
02、Nat Commun | 高碳/脂比饮食可引发不利的代谢改变,该效应与体重无关

饮食在人类健康中发挥着至关重要的作用,而饮食中碳水化合物与脂肪比例(CFR)如何影响代谢组学特征,进而与2型糖尿病风险相关,尚缺乏系统研究。本研究基于弗雷明翰食品研究(FS2)减重维持阶段的数据,纳入164名超重或肥胖成人,随机分配至高、中、低碳水化合物饮食(碳水分别为60%、40%、20%;脂肪供能比分别为20%、40%、60%;),进行为期20周的干预,旨在探讨不同CFR饮食对血浆代谢组的调控作用及其与T2D风险的关联。
1、首先采用液相色谱-串联质谱技术对147名完成干预者的空腹血浆样本进行代谢组学检测,共鉴定出479种代谢物。经多重校正后发现,148种代谢物与CFR水平显著相关。其中,87种代谢物随CFR升高而显著降低,主要包括磷脂酰胆碱、缩醛磷脂、磷脂酰乙醇胺、鞘磷脂、氨基酸、脂肪酸及酰基肉碱;61种代谢物随CFR升高而显著上升,以溶血磷脂酰胆碱、溶血磷脂酰乙醇胺、甘油三酯及甘油二酯为主。
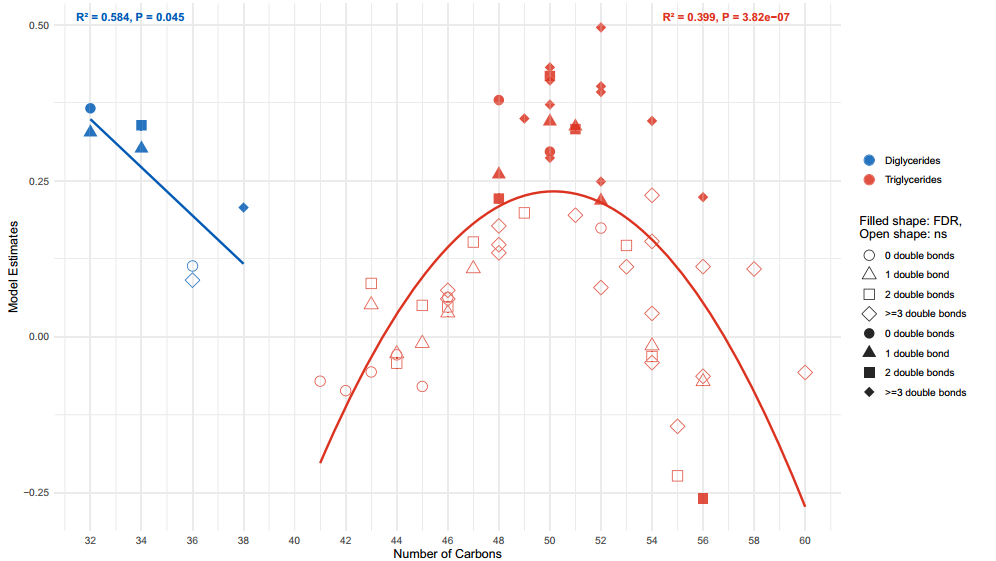
2、随后对甘油三酯和甘油二酯的碳链长度与不饱和度进行分析,发现CFR与甘油三酯呈非线性正相关,其碳链长度集中在48至56之间;与甘油二酯呈线性负相关。所有显著变化的脂肪酸均为饱和脂肪酸,提示CFR对脂质分子的结构特征具有选择性调控作用。
3、通过比较干预早期(10周)与全程(20周)的代谢变化,发现多数代谢物在早期即出现显著变化并持续至全程,但部分酰基肉碱和脂肪酸仅在早期显著,提示机体可能存在代谢适应现象。采用PLS-DA模型分析发现,基于代谢物的饮食类型预测准确率在体重维持者中更高,表明代谢物可有效反映饮食依从性。
4、最后,结合已发表的T2D风险代谢物meta分析数据,发现20种随CFR升高(高碳水低脂肪)而上升的代谢物同样与T2D风险升高相关,绝大多数属于甘油三酯和甘油二酯类。代谢物集合富集分析显示,双键数≤3的甘油三酯在CFR与T2D之间的关联尤为显著,而鞘磷脂则呈反向富集,提示不同脂类在饮食与疾病之间可能扮演不同角色。
参考文献:Angelidi AM, Bartell E, Huang Y, Z, et al. Weight-independent effects of dietary carbohydrate-to-fat ratio on metabolomic profiles: secondary outcomes of a 5-month randomized controlled feeding trial. Nat Commun. 2026.
03、Journal of Hepatology | 生酮与非生酮减重饮食对MASLD肝脏脂肪变性和线粒体代谢的不同影响

代谢功能障碍相关脂肪性肝病(MASLD)发病率不断上升,减肥是目前最有效的治疗手段。然而,不同饮食模式在改善肝脂方面的效果仍存在争议生酮饮食在降低肝脂方面可能优于传统低热量饮食,但其潜在代谢机制尚不清楚,特别是肝脏作为脂肪代谢的核心器官,在生酮状态下线粒体功能怎么变化、脂肪酸被氧化后代谢去向,这些关键环节还缺乏系统研究。基于此,本研究开展了相关探索,得到以下结果:
1、肝脂的降幅差异显著:同等热量限制下,生酮饮食(KD)使肝内甘油三酯(IHTG)下降29%,非生酮饮食(ND)仅降20%,KD效果高出45%。
2、胰岛素敏感性改善不均:KD使血清胰岛素浓度骤降54%,肝胰岛素抵抗(HOMA-IR)改善59%,而ND仅改善21%,二者相差近3倍。
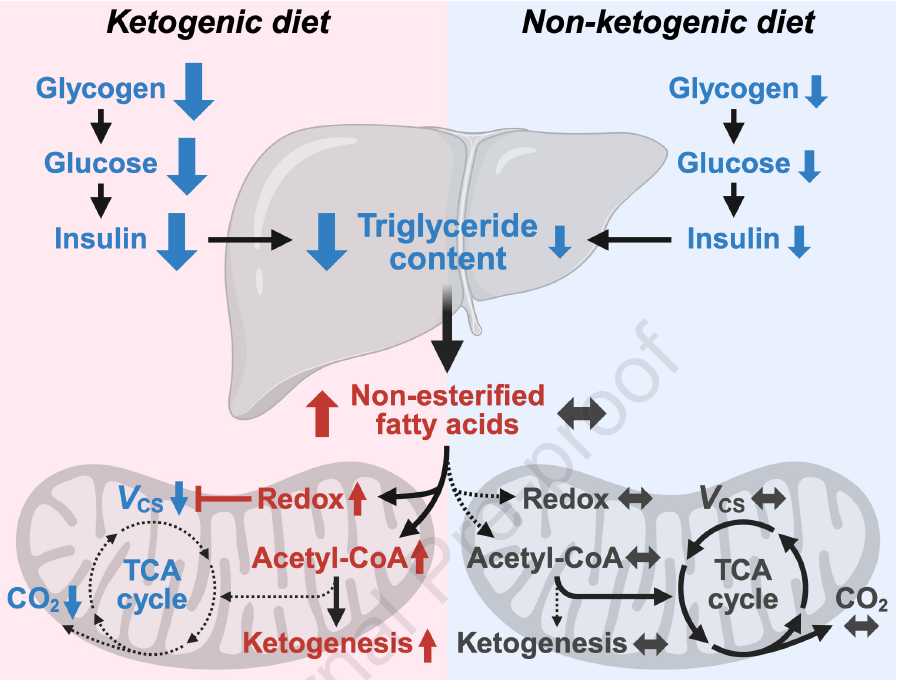
3、线粒体代谢路径分化:KD显著抑制肝脏三羧酸循环氧化率(VCS下降34%),同时酮体生成量增加约250%;ND则无明显变化。
4、氧化还原状态偏移:KD使肝脏线粒体[NADH]/[NAD⁺]比值升高51%,呈现”还原应激”特征,ND保持相对稳定。
5、代谢组学特征迥异:KD特异性升高支链氨基酸、乙酰肉碱和柠檬酸水平,ND则主要降低常规脂代谢指标,显示两种饮食模式具有显著不同的代谢特征。
参考文献:Qadri, S. F., Porthan, K., Dufour, S., et al. (2026). Distinct effects of ketogenic and non-ketogenic weight-loss diets on hepatic steatosis and mitochondrial metabolism in MASLD. Journal of Hepatology. 2026
04、Nature Comunications | SLC6A6将牛磺酸转运至线粒体以维持线粒体翻译和肿瘤生长

牛磺酸是一种含硫氨基酸,在细胞里参与多种保护性功能,比如调节渗透压、抗氧化、稳定细胞膜等。过去的研究主要关注它在细胞质和细胞膜上的作用,但近年发现牛磺酸对线粒体功能也至关重要——它参与修饰线粒体tRNA上的特定核苷酸,从而影响线粒体基因组的翻译效率,进而影响电子传递链的完整性。牛磺酸必须进入线粒体才能发挥这一作用,但具体由哪种转运蛋白介导仍不明确。与此同时,肿瘤细胞高度依赖线粒体代谢来维持快速增殖,而牛磺酸转运蛋白SLC6A6在多种癌症中高表达且与患者预后不良相关。这些线索提示,研究牛磺酸如何进入线粒体,可能为癌症治疗找到新的突破口。基于这个背景,本研究得以展开,得到以下结果:
1、外源牛磺酸非必需:在无牛磺酸培养基中,肝癌和肺癌细胞仍可通过内源合成途径(CDO1-CSAD和ADO通路)维持生长,敲低相关合成酶后细胞增殖才显著受抑。
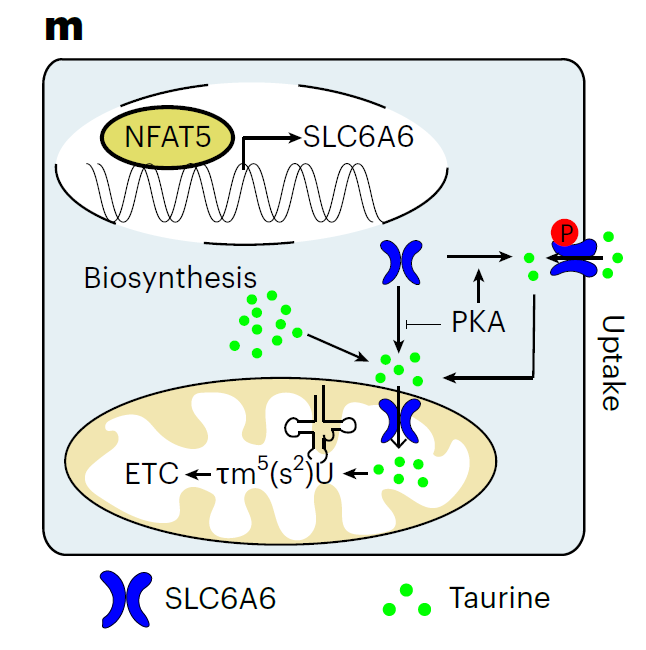
2、SLC6A6定位线粒体膜:传统认为SLC6A6是质膜转运蛋白,但研究发现其N端含线粒体靶向序列,可定位于线粒体内膜,介导胞质牛磺酸向线粒体转运。
3、线粒体牛磺酸耗竭阻断翻译:敲低SLC6A6导致线粒体牛磺酸特异性减少(胞质水平不变),mtRNA的τm⁵U修饰水平骤降,线粒体翻译受阻,电子传递链复合物合成不足。
4、PKA调控亚细胞定位:蛋白激酶A通过磷酸化SLC6A6的Ser21/25位点,促进其质膜定位、抑制线粒体定位;激活PKA可降低线粒体牛磺酸供应并抑制细胞增殖。
5、NFAT5-SLC6A6轴成药靶点:转录因子NFAT5直接结合SLC6A6启动子驱动其表达,小分子抑制剂KRN2靶向该轴可显著抑制多种移植瘤生长并延长肺癌模型小鼠生存期。
参考文献:SLC6A6 imports taurine into mitochondria to sustain mitochondrial translation and tumour growth. Nature Metabolism. 2026.
05、GUT | 揭示人类肠道菌Dysosmobacter welbionis将肌醇转化为丁酸盐的独特途径及其益生菌潜力

丁酸盐是一种对代谢和肝脏健康至关重要的肠道菌群代谢产物。Dysosmobacter welbionis是一种新发现的产丁酸盐细菌,但其在代谢功能障碍相关脂肪性肝病(MASLD)个体中的丰度是否减少尚不清楚。目前对来自水果、豆类、谷物和坚果的膳食成分—肌醇(myo-inositol)发酵产丁酸盐的机制认识也有限。因此,本研究旨在评估菌D. welbionis 在人群中的分布、相对丰度和菌株多样性,并且首次系统解析了这条非经典的肌醇至丁酸盐发酵途径,并鉴定了相关候选基因。
1、分析多个人类队列发现,菌D. welbionis是人类肠道中普遍存在的细菌。在两个MASLD患者队列中,其丰度显著降低。在饮食诱导脂肪肝的小鼠模型中,补充 D. welbionis J115T 改善了高血糖并减轻了肝脏脂肪变性。
2、通过表型芯片筛选碳源,利用13C标记的肌醇同位素结合核磁共振(NMR)、质谱、蛋白质组学和基因组学技术,解析其代谢路径。结果表明,肌醇是支持 D. welbionis J115T 生长的关键碳源之一,该菌能特异性地将肌醇发酵为丁酸盐和乙酸盐。蛋白质组学分析表明,该途径中的酶在肌醇生长条件下被特异性诱导。
3、采用抗体引导的厌氧细胞分选技术从人类粪便中成功分离了19株新的D. welbionis菌株。比较基因组学显示,该物种拥有开放的泛基因组,但将肌醇转化为丁酸盐的完整途径在所有菌株中高度保守。抗生素耐药基因分析鉴定出两株不携带预测耐药基因的菌株,具有作为安全益生菌候选的潜力。
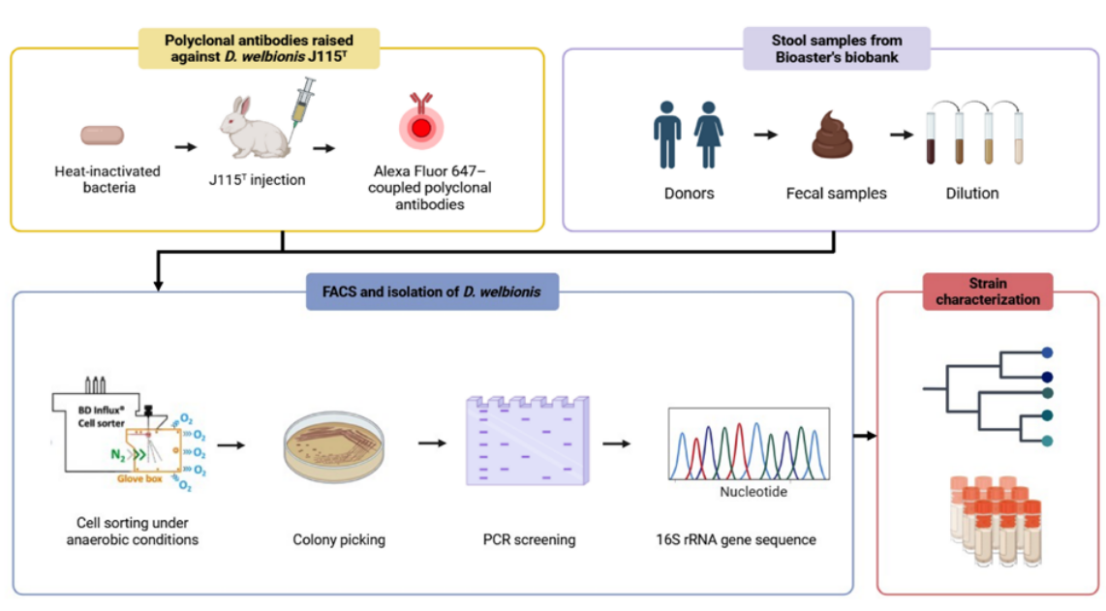
参考文献:Lee CH, et al. Novel myo-inositol to butyrate fermentation pathway in the prevalent human gut species Dysosmobacter welbionis, a bacterium associated with improved metabolic and liver health. Gut. 2026.
06、GUT | A. baumannii通过烟酸介导的NAD代谢重编程和糖酵解激活促进胃癌转移

胃癌是全球常见的恶性肿瘤。虽然幽门螺杆菌是公认的致癌因子,但其在肿瘤组织中的丰度下降,提示其他微生物可能在胃癌进展中起作用,但其机制尚不明确。先前研究发现,胃癌组织中 Acinetobacter baumannii的丰度显著升高。本研究旨在探究A. baumannii是否及如何影响胃癌的转移。
1、qPCR定量结果表明,A. baumannii在胃癌组织(尤其是晚期)中丰度显著高于正常组织,且与TNM分期正相关。荧光原位杂交(FISH)分析证实其在肿瘤内定植,该菌对胃癌细胞表现出更强的粘附能力。
2、通过体内(裸鼠肝/腹膜转移模型)和体外(划痕、Transwell实验)验证A. baumannii促胃癌细胞转移功能。代谢学分析发现菌株丰度与组织内烟酸和1-甲基烟酰胺水平正相关。敲除pncA基因后,细菌产生烟酸和促转移的能力丧失。
3、代谢组检测表明,A. baumannii及其代谢物(烟酸和1-甲基烟酰胺)处理导致胃癌细胞内NAD+水平升高、NAD+/NADH比率下降,并引起糖酵解增强。RNA-seq和蛋白分析显示,HIF-1α信号通路及其下游的糖酵解酶(如GLUT1、HK2)和上皮-间质转化(EMT)标志物被显著激活。
4、敲低HIF-1α或使用抑制剂,能显著抑制A. baumannii及其代谢物所诱导的细胞迁移、体内转移以及HIF-1和EMT通路的激活。
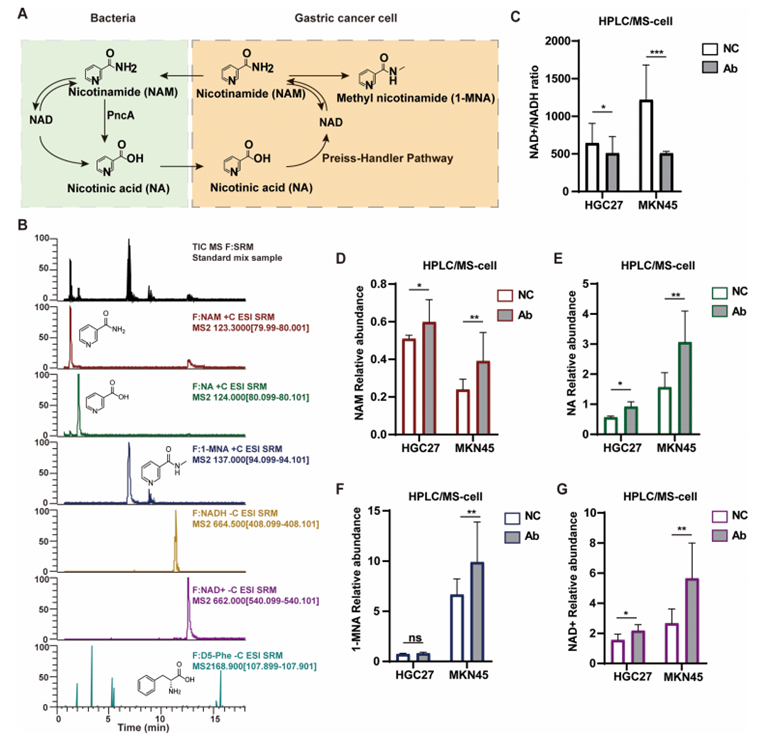
参考文献:Yang Y, et al. Acinetobacter baumannii promotes gastric cancer metastasis via NA-mediated NAD metabolism reprogramming and glycolytic activation. Gut. 2026.
07、Gut | 犬尿喹啉酸通过肠脑神经环路减轻卒中后的脑损伤

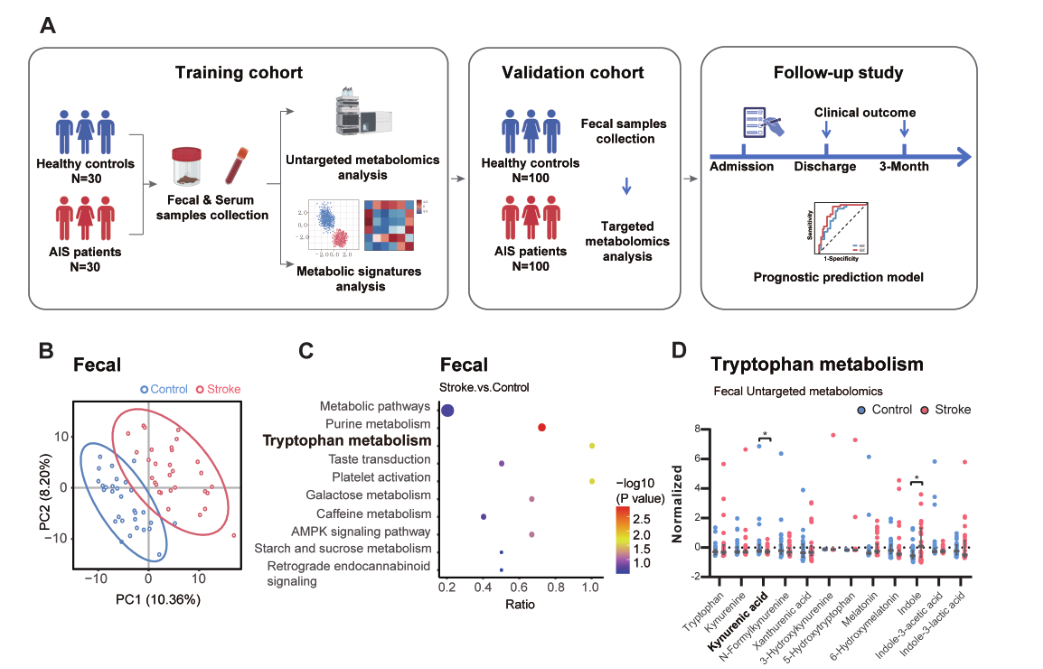
卒中是全球范围内致死致残的主要原因,缺血性卒中占比极高,现有急性干预手段仍难以有效降低其死亡率与致残率,亟需挖掘新的发病机制及治疗靶点。肠-脑轴可通过代谢、免疫及神经途径调控中枢神经系统稳态,肠道代谢物被证实参与卒中病程调控,但肠道信号调控卒中后脑损伤与恢复的具体神经环路机制尚未明确。本研究通过代谢组学、临床队列分析以及动物模型干预发现KYNA(犬尿喹啉酸)通过G蛋白偶联受体35(GPR35)-迷走神经回路发挥作用,为卒中治疗和神经功能恢复提供了新的潜在靶点。
1、通过非靶向代谢组学分析发现,AIS(急性缺血性卒中)患者粪便样本中色氨酸(TRP)代谢显著改变,犬尿喹啉酸(KYNA)水平显著降低,且肠道KYNA水平与患者入院NIHSS评分、出院NIHSS评分、3个月mRS评分均呈强负相关。靶向代谢组学分析进一步证实了AIS患者粪便中KYNA的显著减少。
2、通过不同的给药方式以及剂量梯度实验发现,仅胃肠道灌胃KYNA可显著降低卒中后3天小鼠的脑梗死面积、改善神经功能评分,且低、中剂量可显著改善卒中损伤。
3、进一步通过分子对接、细胞实验、体内基因操作等实验发现,KYNA通过特异性激活肠神经元上的GPR35受体发挥作用。
4、通过体内外实验进一步验证了KYNA通过特异性激活肠神经元上的GPR35受体,启动迷走神经介导的肠-脑神经环路,发挥卒中后神经保护作用。
参考文献:Zhang W, Chen S, Huang X, et al. Kynurenic acid mitigates poststroke brain damage through the gut-brain neural circuit. Gut. 2026.
08、Cell Metabolism | 微生物代谢产物FAD能促使脂肪细胞进行脂质重塑,提升癌症免疫治疗效果

免疫检查点阻断(ICB)是癌症治疗的重要手段,且疗效存在显著个体差异,肠道微生物群与脂肪组织之间的相互作用对癌症患者的免疫治疗反应有着至关重要的影响,但其背后机制尚不明确。本研究发现,肥胖患者体内富集的产核黄素菌群会提升黄素腺嘌呤二核苷酸(FAD)水平,进而激活脂肪细胞中FADS2介导的多不饱和脂肪酸(PUFAs)合成。粪菌移植、补充关键菌株或DHA等干预可恢复并提升ICB疗效,为优化癌症免疫治疗提供新策略。
1、通过宏基因组分析发现,在体重指数(BMI)≥25的癌症患者(对免疫检查点抑制剂(ICB)治疗有反应)中,有六种细菌种类的含量显著增加,其中包括Eubacterium rectale、Adlercreutzia equolifaciens、Megamonas hypermegale、Lachnospiraceae bacterium (5_1_63FAA)、Gordonibacter pamelaeae和Citrobacter freundii。 前五种菌进一步在独立验证队列中得到验证。
2、通过功能分析进一步发现,在BMI≥25的应答者中,辅因子代谢途径显著上调。
3、通过高效液相色谱-质谱分析,FAD的水平在ICB应答者中显著高于非答者,而S-腺苷甲硫氨酸、硫胺素和烟酸的水平未见明显差异。
4、通过单细胞RNA测序(scRNA-seq)和流式细胞术发现,与FMT低剂量组相比,FMT高剂量组中与T细胞细胞毒功能相关的多个基因(如Ifng和Gzmk)的表达显著升高,且FAD干预后肿瘤浸润CD8+T细胞比例显著升高。
5、通过代谢组学分析发现,不饱和脂肪酸的生物合成途径在FAD和抗PD-1联合治疗组显著富集,且DHA最重要的脂质标志物。进一步实验发现,补充DHA可增强瘦小鼠的抗PD-1反应,促进CD8+T细胞的IFN-γ分泌。
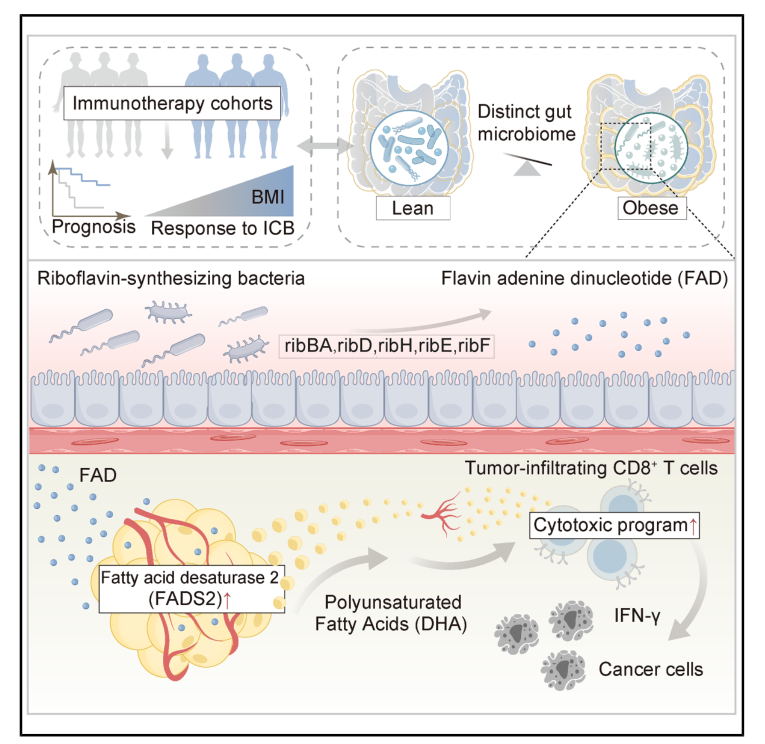
参考文献:Tong T, Huang X, Li L, et al. Microbial metabolite FAD mobilizes adipocyte lipid remodeling to enhance cancer immunotherapy efficacy. Cell Metablism. 2026.
END


