文献解读
Nature | 促癌亦增敏:ATF6α驱动糖代谢重编程,塑造肝癌免疫微环境
肝细胞癌(HCC)约占原发性肝癌的80%-85%,主要源于慢性肝炎中恶性转化的肝细胞。尽管免疫疗法改善了患者生存,但遗传、代谢与炎症的复杂交互作用仍是有效治疗的主要障碍。浸润肝癌的淋巴细胞表达PD-1、CTLA-4等耗竭产物,导致患者预后不良。目前,免疫检查点阻断(阿替利珠单抗)联合VEGF阻断(贝伐珠单抗)已成为不可切除肝细胞癌的标准治疗方案,但代谢相关的肿瘤逃逸与免疫抑制仍期待新突破。
内质网应激及其触发的未折叠蛋白反应激活是癌症的预后差的原因之一,涉及三条信号通路:PKR样内质网激酶(PERK)、肌醇需求酶1α(IRE1α)及活化转录因子6α(ATF6α)。其中,ATF6α经剪切生成N端p50片段(nATF6α)后入核,激活内质网伴侣蛋白及脂质合成相关基因。尽管PERK和IRE1α已被证实可促进癌症特征性变化,但ATF6α在肝癌中的作用尚不明确。
2026年2月,美国桑福德·伯纳姆·普雷比斯医学发现研究所、德国慕尼黑工业大学、德国癌症研究中心联合在Nature上发表了题为Activated ATF6α is a hepatic tumour driver restricting immunosurveillance的研究论文,指出ATF6α通过抑制FBP1驱动代谢重编程与免疫抑制,在促进肝癌发生的同时也使肿瘤对免疫检查点阻断疗法敏感,从而揭示了ATF6α在肝细胞癌中的双重作用。

技术路线

研究结果
1、ATF6α的激活与肝细胞癌密切相关
为探究ATF6α在人类肝细胞癌中的作用,研究者首先研究了患者的病理组织切片,发现慢性肝炎患者的肝细胞核内存在ATF6α表达,提示病理状态下内质网应激可诱导ATF6α激活。为验证这一发现的普遍性,进一步整合分析了22个独立的人类肝细胞癌数据集。结果显示,无论在mRNA水平还是特征基因集评分层面,ATF6α的激活在肝癌组织中均显著高于非肿瘤肝脏组织。进一步基于癌症基因组图谱(TCGA)肝细胞癌数据的分析表明,ATF6α激活与患者总生存期缩短显著相关,且这一相关性为ATF6α所特有,提示其可能是肝细胞癌独特且关键的驱动因素。
随后,根据ATF6α激活特征对患者进行分层分析,发现高激活特征的肿瘤在肝祖细胞转化、细胞周期进展及癌发生等标志性通路上显著富集,而代谢相关通路评分则较低。对中国人群肝癌蛋白质组学数据的评估进一步显示,预后最差的患者亚群(SIII)的肿瘤中,ATF6α靶标和糖酵解相关蛋白表达增加,而糖异生关键酶FBP1的表达显著降低,同时伴随增殖、免疫抑制和转移相关蛋白的富集。免疫印迹分析证实,有活性的裂解形式ATF6α(nATF6α)在肿瘤组织中优先积累,且定位于肝细胞核,无活性的全长ATF6α则保留在胞质中。
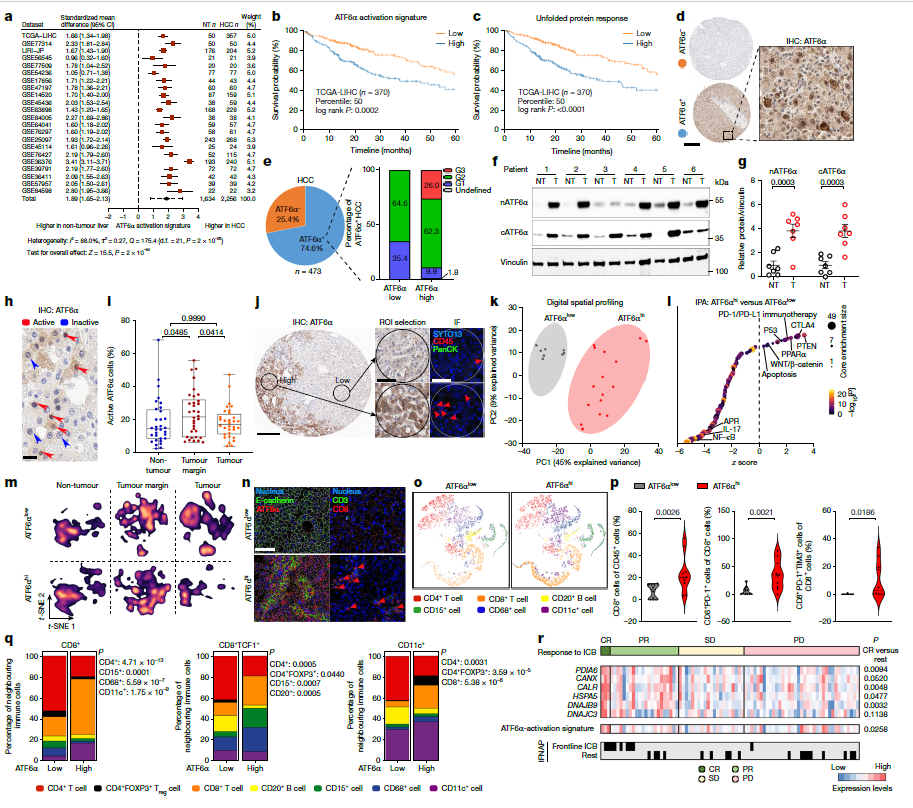
图1. 肝脏ATF6α的激活是HCC患者的预后因素
以上结果表明,ATF6α的激活,特别是其活性形式的核转位,是侵袭性肝癌的重要标志。
2、ATF6α通过抑制FBP1诱导肝损伤
为在活体水平验证上述发现,研究者构建了肝细胞特异性激活ATF6α的转基因小鼠模型(TGAlb-cre+)。与对照组相比,TGAlb-cre+小鼠呈现明显的肝肿大和肝损伤,表现为肝重比增加、血清转氨酶水平升高。透射电子显微镜观察显示,其肝细胞出现明显的内质网肿胀和结构破坏,证实了强烈的内质网应激。分子水平上,未折叠蛋白反应靶标、细胞增殖标志物、DNA损伤标志物及癌胚蛋白AFP的表达均显著上调。转录组和蛋白质组分析进一步揭示,ATF6α的激活上调了未折叠蛋白反应、糖酵解、炎症和致癌信号通路,同时下调了氧化磷酸化和脂肪酸代谢。
在靶基因层面,研究者发现糖异生限速酶FBP1的表达在mRNA和蛋白水平均被显著抑制。CUT&RUN实验证实,nATF6α可直接结合于Fbp1基因启动子区域,且该区域的染色质可及性随之降低,表明ATF6α激活直接导致了Fbp1基因座的染色质闭合与转录抑制。为验证FBP1下调在其中的关键作用,研究者在TGAlb-cre+小鼠中恢复了FBP1表达。结果显示,FBP1的重新表达可逆转ATF6α激活所诱发的肝损伤,在分子层面抑制了糖酵解,减轻了内质网应激和DNA损伤,同时促进了糖异生,恢复了肝脏糖原水平。
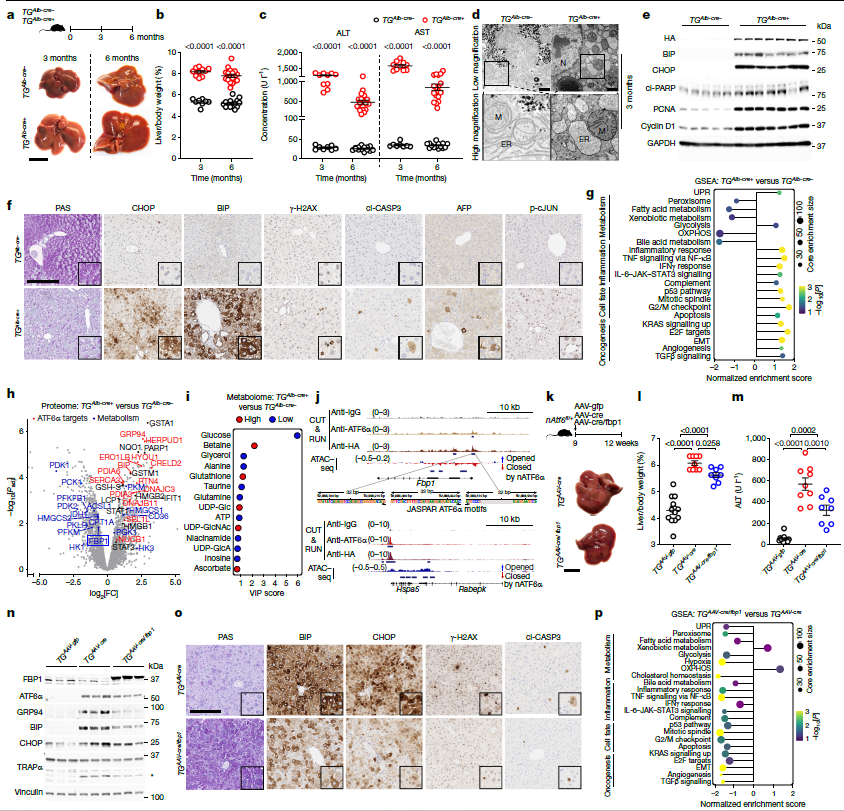
图2. 肝细胞中持续的ATF6α激活通过抑制FBP1诱导肝损伤和糖代谢功能障碍
以上结果表明,ATF6α激活驱动的肝损伤和代谢重编程,主要通过抑制具有催化活性的FBP1来实现。
3、肝细胞中持续的ATF6α激活会诱导肝癌
基于慢性肝炎向肝癌进展的临床病理学基础,研究者进一步探究ATF6α持续激活是否足以驱动肝癌发生。长期观察显示,TGAlb-cre+小鼠的生存期显著缩短,并自发形成肝脏肿瘤。影像学及病理学证实,这些肿瘤绝大多数为肝细胞癌,且伴有ATF6α的持续性核定位。染色体畸变分析表明,上述小鼠来源的肝癌具有与人类肝癌相当的基因组不稳定性。
在化学致癌物(DEN)联合高脂饮食(HFD)诱导的加速肝癌模型中,ATF6α的激活同样显著增加了肿瘤数量、大小及发生率。转录组分析进一步证实,ATF6α激活的肿瘤中内质网应激、炎症及致癌信号通路增强,同时Fbp1表达下调。
将小鼠模型中定义的ATF6α激活特征映射至人类肝癌数据集后发现,该特征与人类ATF6α激活特征、内质网应激及免疫耗竭等特征高度相关。在人类肝癌样本中,FBP1 mRNA水平与ATF6α激活特征呈显著负相关,进一步验证了上述发现的临床相关性。
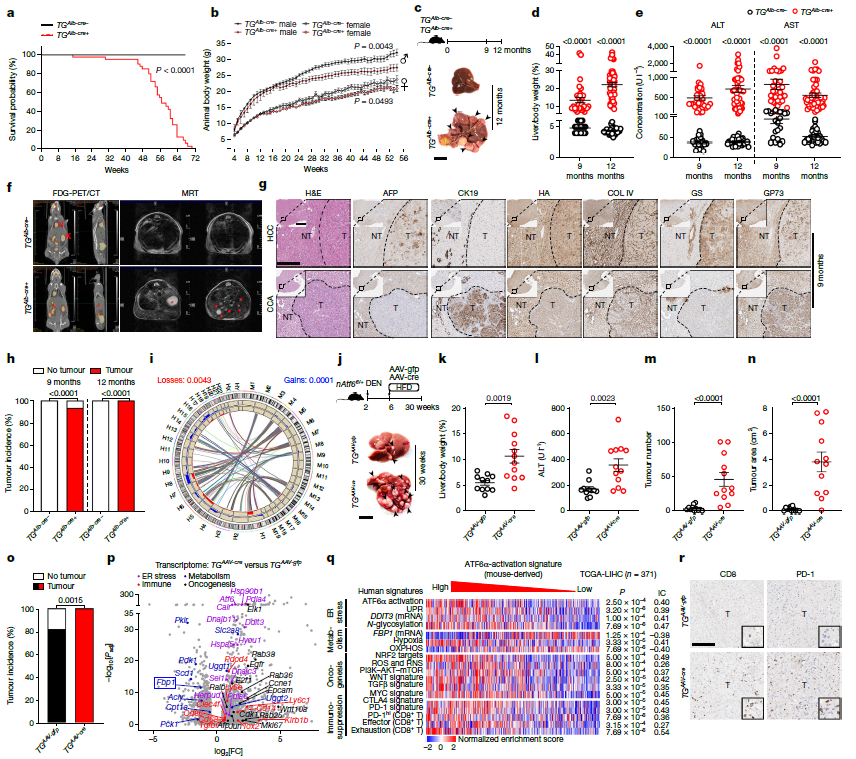
图3. 持续的ATF6α激活诱导小鼠原发性肝癌
4、靶向抑制ATF6α可有效减少肿瘤负荷
为验证ATF6α在肝癌发生中的必要性,研究者采用多种策略在递进的小鼠模型中开展验证。从化学诱导模型的全身性敲除,到精准定位肝细胞的特异性敲除,再到内质网应激驱动的MUP-uPA遗传模型,三种小鼠模型一致证实:抑制ATF6α可有效减轻肝损伤、降低肿瘤负荷,且这一保护效应独立于肝癌的致病诱因。分子机制层面,转录组与代谢分析显示,Atf6缺失可恢复Fbp1表达、抑制糖酵解并增加肝脏葡萄糖含量。
基于上述发现,研究者进一步探索ATF6α的治疗潜力,利用可被肝细胞特异性摄取的GalNac偶联反义寡核苷酸(ASO-Atf6)靶向敲低Atf6表达。在MUP-uPA模型中,无论早期预防性给药还是肿瘤形成后的晚期治疗,ASO-Atf6均能有效减轻肝损伤、缓解内质网应激与糖原耗竭,并显著降低肿瘤负荷。在另一由突变型NRASG12V质粒快速诱导的肝癌模型中,ASO-Atf6同样减小肿瘤体积、阻止糖原耗竭,并减少PD-1+细胞浸润。
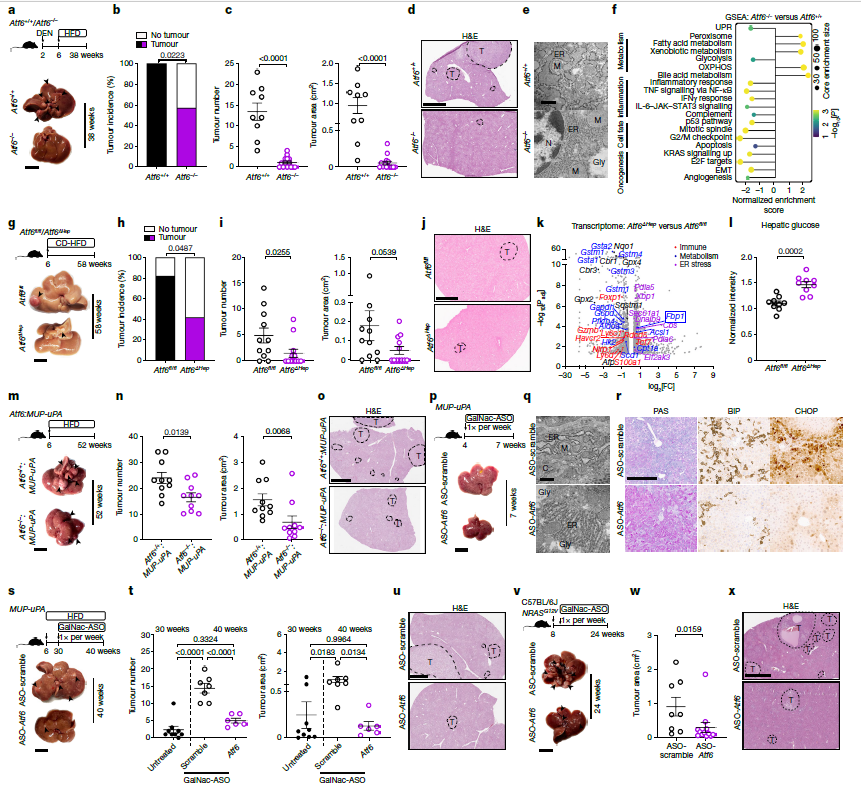
图4. 预防性或治疗性靶向Atf6可减少肝细胞癌
以上结果从遗传学与药理学角度共同证实,ATF6α是肝癌发生的关键驱动因素,亦是一个极具潜力的治疗靶点。
5、肝细胞ATF6α的激活具有双重作用
研究者发现,在TGAlb-cre+小鼠的癌前肝脏中就已经形成了免疫抑制环境:髓源性抑制细胞、PD-1+T细胞及M2型巨噬细胞浸润增加,PD-L1表达上调。换言之,早在肿瘤发生之前,ATF6α的激活已驱动肝脏微环境向免疫抑制方向重塑。单细胞RNA测序分析显示,在ATF6α激活的肝脏中,CD8+T细胞的糖酵解与氧化磷酸化通路活性均显著低于对照组。代谢能力的下降导致这些细胞虽向效应甚至耗竭状态分化,却无法维持正常的抗肿瘤功能。这可能是由于ATF6α激活的肝细胞过度摄取葡萄糖,造成了微环境能量匮乏,同时其释放的乳酸进一步加剧T细胞代谢压力导致的。体外共培养实验证实,表达活性ATF6α的肝癌细胞对T细胞杀伤具有更强的抵抗力,而抑制乳酸代谢可部分恢复T细胞功能。
有趣的是,ATF6α激活在驱动免疫抑制的同时,却也塑造了一个对免疫检查点阻断(ICB)疗法可能敏感的肿瘤微环境。研究者发现,在ATF6α高表达的肝癌区域,尽管存在更多耗竭的CD8+T细胞,但其中同时富集了对ICB有反应的TCF1+ progenitor exhausted T细胞,且这些细胞与抑制性Treg细胞在空间上相互分离。回顾性分析进一步支持这一关联:在接受抗PD-1单药治疗的晚期肝癌患者中,达到完全缓解者的肿瘤组织呈现显著更高的ATF6α靶基因表达及激活特征评分,提示ATF6α激活状态或可作为预测ICB疗效的生物标志物。
为了验证这一假设,研究者首先对荷瘤TGAlb-cre+小鼠进行抗PD-1抗体治疗。结果显示,阻断PD-1显著减少了肿瘤数量与大小,同时增加了肿瘤内CD8+T细胞浸润及其糖酵解关键酶LDH的表达。进一步地,在原本对ICB不敏感的MYC:TP53KO诱导肝癌模型中,人为激活ATF6α后,肿瘤对后续抗PD-1治疗也转为敏感。最后,通过构建PD-1基因缺失的TGAlb-cre+小鼠模型,从遗传学层面彻底阻断PD-1信号,同样观察到肿瘤发生被抑制、生存期延长的保护效应。
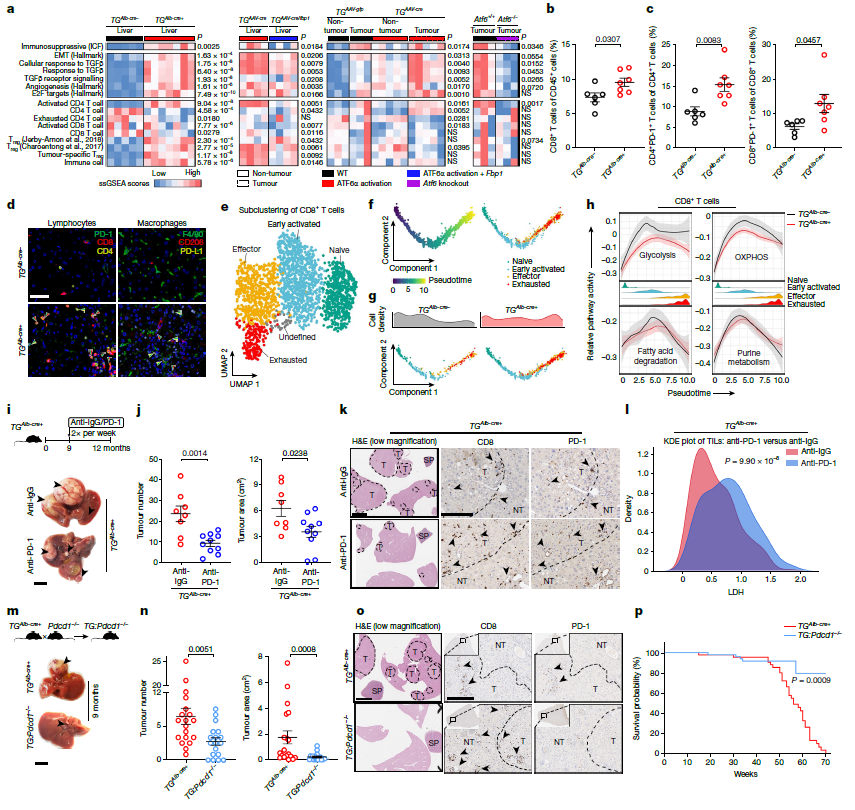
图5. 肝细胞ATF6α激活通过代谢途径限制抗肿瘤免疫监视
以上结果共同证明,ATF6α激活虽驱动肝癌发生并塑造免疫抑制微环境,却也正是这种独特的微环境,尤其是其中富含耗竭但可被再激活的T细胞亚群,使得该类肿瘤对免疫检查点阻断疗法高度敏感。
全文总结
本研究确立了ATF6α作为肝细胞癌的关键驱动因子的全新功能,揭示了其通过转录抑制FBP1驱动代谢重编程、进而塑造免疫抑制微环境的核心机制。更重要的是,研究发现ATF6α激活虽促进肿瘤发生,却也使肿瘤对免疫检查点阻断疗法高度敏感,提示ATF6α激活状态可作为预测ICB疗效的生物标志物。靶向ATF6α及其下游代谢通路,或联合免疫检查点阻断,有望成为肝癌预防与治疗的新策略。
参考文献
Li X, Lebeaupin C, Kadianaki A, et al. Activated ATF6α is a hepatic tumour driver restricting immunosurveillance. Nature. 2026.
请扫描二维码阅读原文

绘谱帮你测
麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱已为数百家三甲医院、科研院所和企业提供多组学一站式整体解决方案,协助客户与合作伙伴发表SCI文章600+篇,累计影响因子6000+,平均IF>10,涵盖Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等顶级期刊。


