文献解读
The EMBO Journal | 运动产生的α-KG通过OXGR1刺激肌肉肥厚和脂肪分解
肥胖被认为是一种全球性的流行病,在众多肥胖预防策略中,体育运动是最安全和有效的降脂方式之一。不同于其他类型运动,阻力运动对脂肪的减少尤其是肌肉的肥厚有促进作用,但其机制知之甚少。华南农业大学动物学院江青艳和束刚教授团队利用比较代谢组学方法发现α-酮戊二酸(AKG)的大量积累是小鼠急性阻力运动的血清代谢特征,考察了AKG对正常饮食(chow)或高脂饮食(HFD)小鼠的代谢调节作用,并采用功能丧失和功能获得小鼠模型来确定AKG的抗肥胖作用是否需要由肾上腺表达的2-酮戊二酸受体1(OXGR1)介导,验证了OXGR1对于阻力运动诱发的代谢有益作用是必需的,相关研究成果发表于国际知名期刊《The EMBO Journal》。
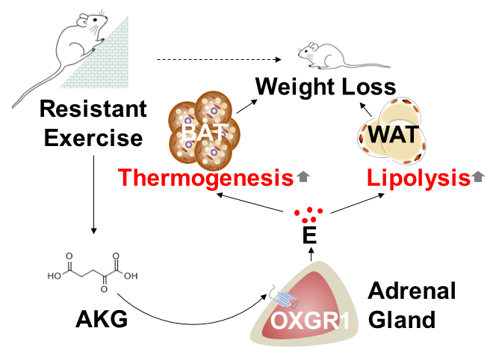
运动引起AKG富集
本研究发现爬梯(阻力)和跑步机(耐力)运动在抑制HFD诱导的体重增加方面具有相似的效果(图1A)。但与耐力运动相比,阻力运动表现出更好的有益代谢作用,如更高的瘦重、更低的脂肪量(图1B)、更低的性腺脂肪组织(gWAT)指数(图1C)。通过非靶向代谢组学测定雄性小鼠阻力运动后血清代谢物变化,发现相比未运动组,运动组高峰期有56种代谢物发生显著变化(图1D),减少的代谢物以氨基酸为主,而增加的代谢物以脂肪酸为主(图1D-E)。停止运动后血浆代谢物变化反映出TCA循环中间体/ AKG相关代谢物的快速上调(图1F)。值得注意的是,血浆AKG浓度与几种代谢危险因素(体重指数(BMI)/臀围(HCF)、腰围、脂肪量和体重)呈显著负相关,提示AKG在体重控制中至关重要。肌肉中AKG水平,胫骨前肌、腓肠肌和比目鱼肌相关酶如谷氨酸脱氢酶(GDH)、α-酮戊二酸脱氢酶(a-KGDH)、异柠檬酸脱氢酶(ICDHm)活性显著增强,表明阻力运动能增强肌肉AKG的合成和血液AKG的释放,进一步提示AKG在运动诱导反应中的重要作用。
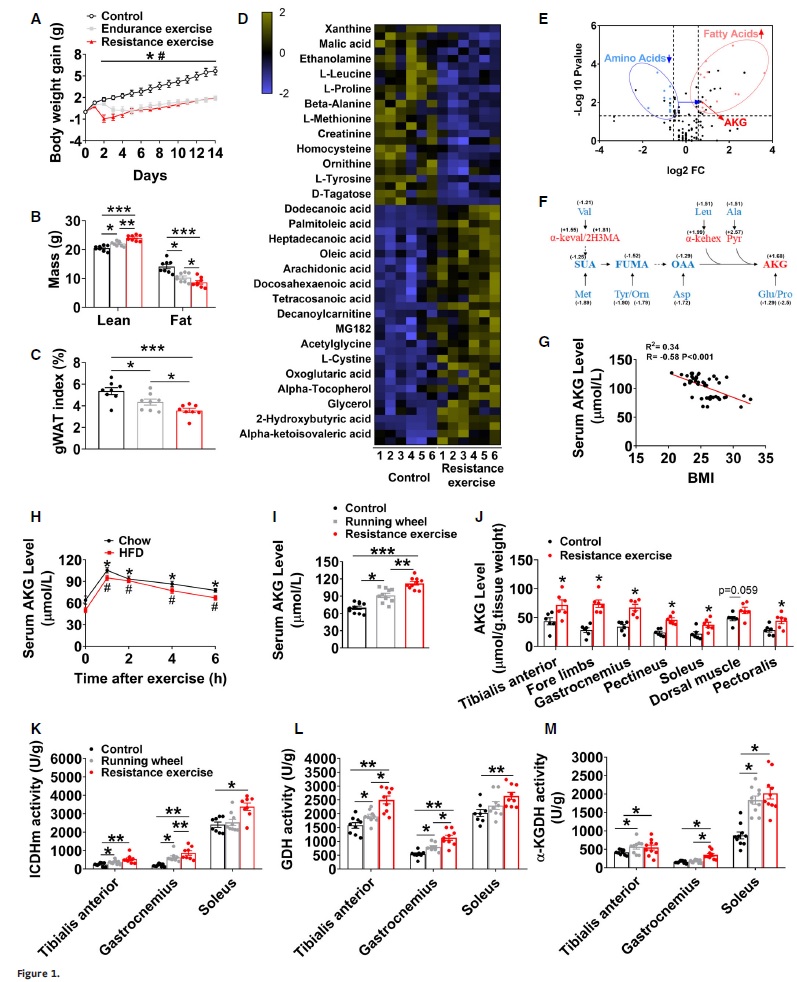
图1. 运动诱导AKG合成
AKG抑制饮食引起的肥胖
运动引起AKG水平出现变化,那么补充AKG是否可以模拟运动造成的某些代谢效应?作者证实急性口服AKG水溶液可导致循环AKG水平升高(图2A)。在HFD饮食诱导肥胖(DIO)模型中补充AKG, AKG处理的雌性和雄性老鼠都表现出水摄入量的增加(图2B和M)、体重增加减少(图2D和O)及食物摄入量相似(图2C和N)、瘦重增加(图2E,F,P和Q)。AKG对HFD诱导的体重增加的抑制作用仅仅是由于脂肪量的减少,即gWAT和iWAT,而不是BAT(图2G-I和R-T),AKG处理的小鼠gWAT和iWAT的平均脂肪细胞大小均显著小于对照组(图2K, L, U和V)。由此表明,AKG在预防HFD引起的体重增加和两性脂肪组织扩张方面具有重要作用。
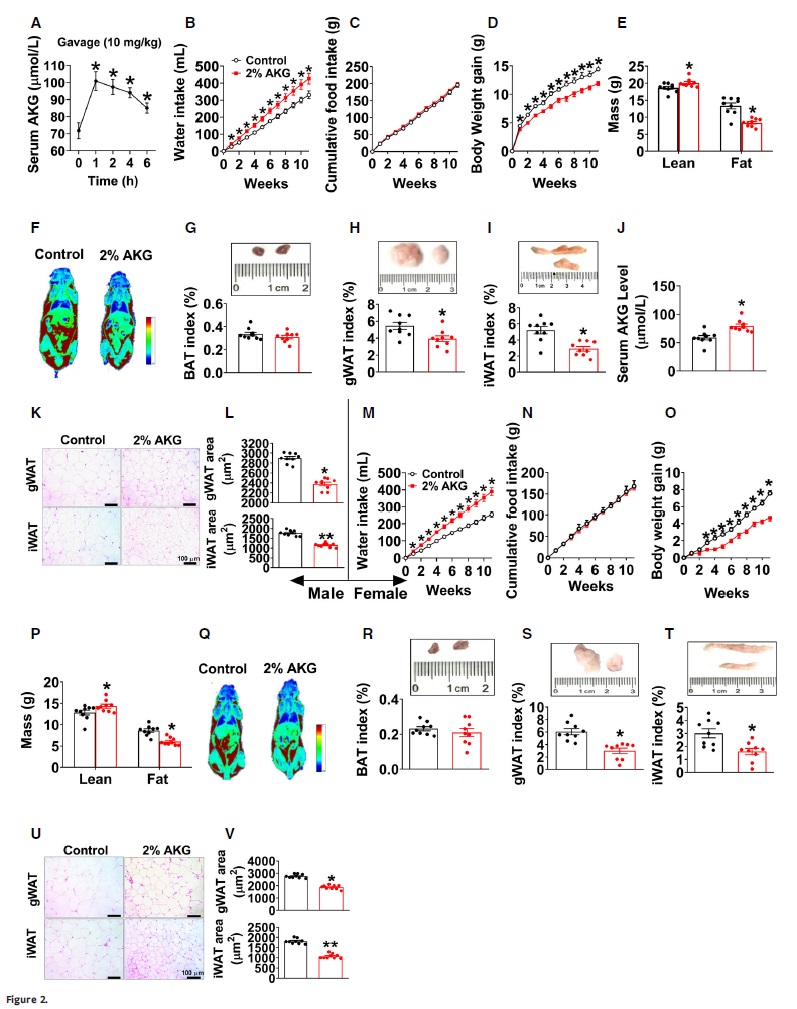
图2. AKG抑制饮食引起的肥胖
AKG促进脂肪产热和脂肪分解
为了确定AKG对DIO的保护作用机制,雄性对照小鼠和AKG处理小鼠被引入间接量热法系统。与对照组相比,AKG处理的小鼠在光/暗周期中都表现出更高的能量消耗(图3A-B)。增强的能量消耗与核心体温(图3C)和冷诱导的BAT温度(图3D和E)的升高有关,表明产热增加。AKG显著增加BAT中解偶联蛋白1 (UCP1)、碘甲状腺素脱碘酶2(Dio2)、细胞死亡诱导DNA片段化因子-α样效应因子A(Cidea)等产热基因的mRNA表达(图3F),其中UCP1蛋白表达升高(图3G-I)。从AKG处理的小鼠WAT中激素敏感性脂肪酶磷酸化(p-HSL)水平升高和脂肪细胞甘油三酯脂肪酶(ATGL)蛋白表达水平升高(图3N-Q),提示呼吸交换率(RER)升高与脂肪分解增强相关,二者都是脂肪细胞中的关键脂肪酶;可见BAT产热和WAT脂解均受代谢激素的协调控制。此外,AKG显著增加了雄性小鼠的血清儿茶酚胺(E),而NE, T4或T3并未增加,提示AKG引起肾上腺素刺激增加。由此表明,AKG可以刺激BAT热生成和脂肪代谢,从而促进能量消耗预防DIO。
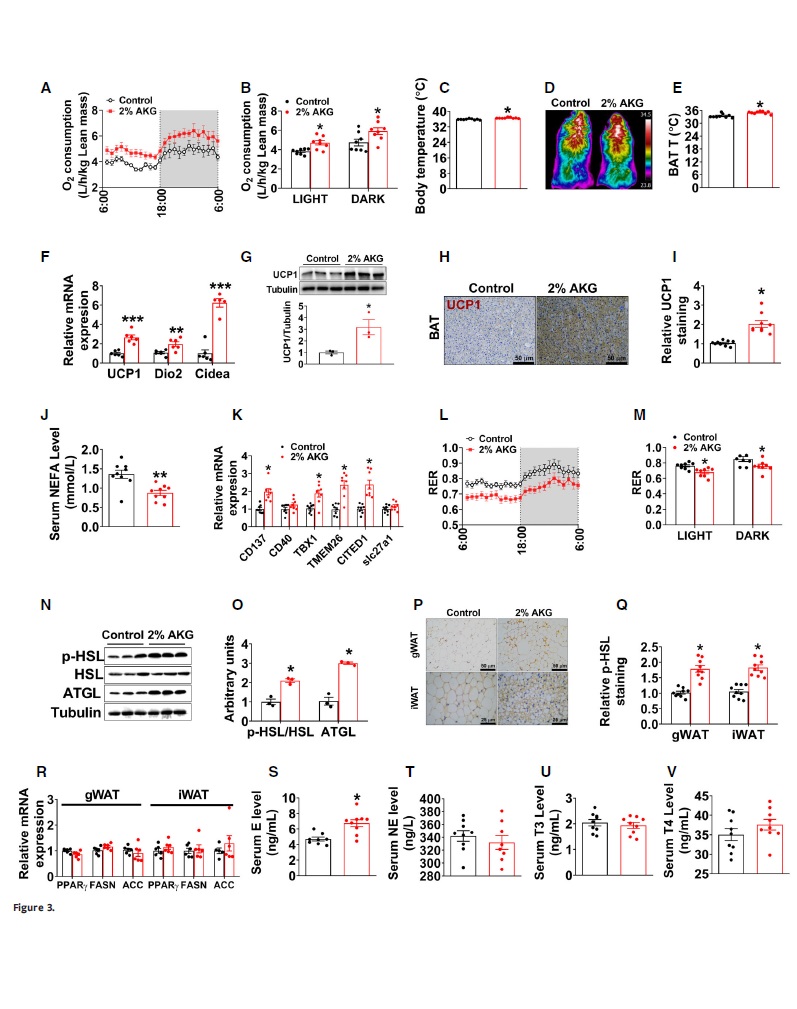
图3. AKG促进脂肪产热和脂肪分解
肾上腺素促进脂肪组织产热和脂解来介导AKG代谢
研究发现与长期补充AKG效果类似,急性腹腔注射AKG也会刺激BAT产热和WAT脂肪分解。在急性和长期AKG处理后,血清E而非NE(图4E)均显著升高,提示AKG诱导肾上腺髓质功能激活。升高的血清E可能介导AKG对BAT产热和WAT脂解的刺激作用。注射β-3肾上腺素能受体(ADRB3)抑制剂SR59230A可抑制AKG调节作用(图4F-I)。肾上腺切除术也可消除AKG的抗肥胖作用(图4J-U)。结果表明,肾上腺在AKG诱导的脂肪组织脂肪代谢和产热中发挥中介作用。
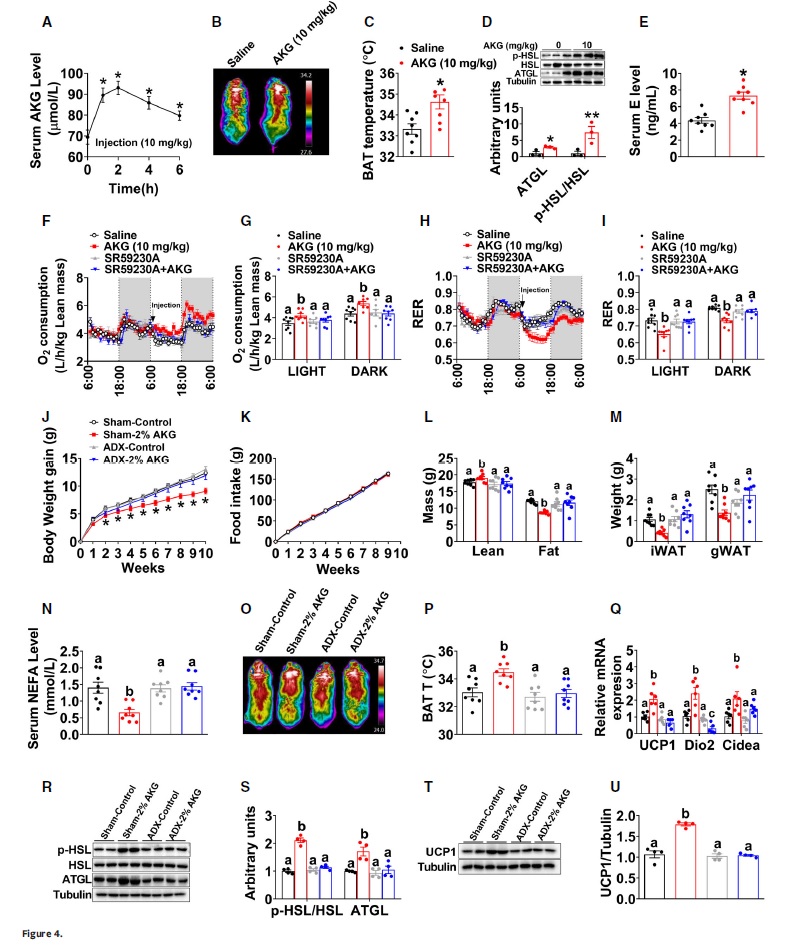
图4. 肾上腺素促进脂肪组织产热和脂解来介导AKG代谢
OXGR1AG是AKG刺激脂肪组织产热和脂肪分解必需的
研究发现肾上腺2-酮戊二酸受体1(OXGR1AG)绝对mRNA表达水平最高(图5A),且除睾丸外远高于其他组织(图5B)。急性AKG治疗和阻力运动中OXGR1AG的mRNA表达均升高(图5D),提示OXGR1AG可能在AKG对肾上腺E释放的直接刺激中起作用。siRNA特异性靶向OXGR1生成功能缺失嗜铬细胞模型,发现OXGR1-敲低嗜铬细胞模型中OXGR1蛋白的表达明显低于siRNA处理的对照组细胞(图5E),而OXGR1的下调可以消除AKG对E分泌的刺激作用(图5F)和瞬时胞内钙的释放(图5G),表明OXGR1AG在AKG诱导的E释放中具有中介作用。CRISPR生成OXGR1整体基因敲除小鼠模型(OXGR1KO)及HBAAV2/9-OXGR1病毒导入OXGR1KO小鼠肾上腺中生成了OXGR1肾上腺选择性表达(OXGR1REAG)小鼠模型,也验证了相关结果。这些结果表明OXGR1AG在AKG对HFD诱导肥胖的抑制作用中起着至关重要的作用,间接量热系统也证明了OXGR1的关键中介作用,进一步证实OXGR1是补充AKG诱导的脂解和产热的关键介质。因此,功能丧失和功能获得模型的结果都表明,OXGR1AG介导了补充AKG诱导的脂肪组织生热和脂肪分解,进而阻止了DIO。
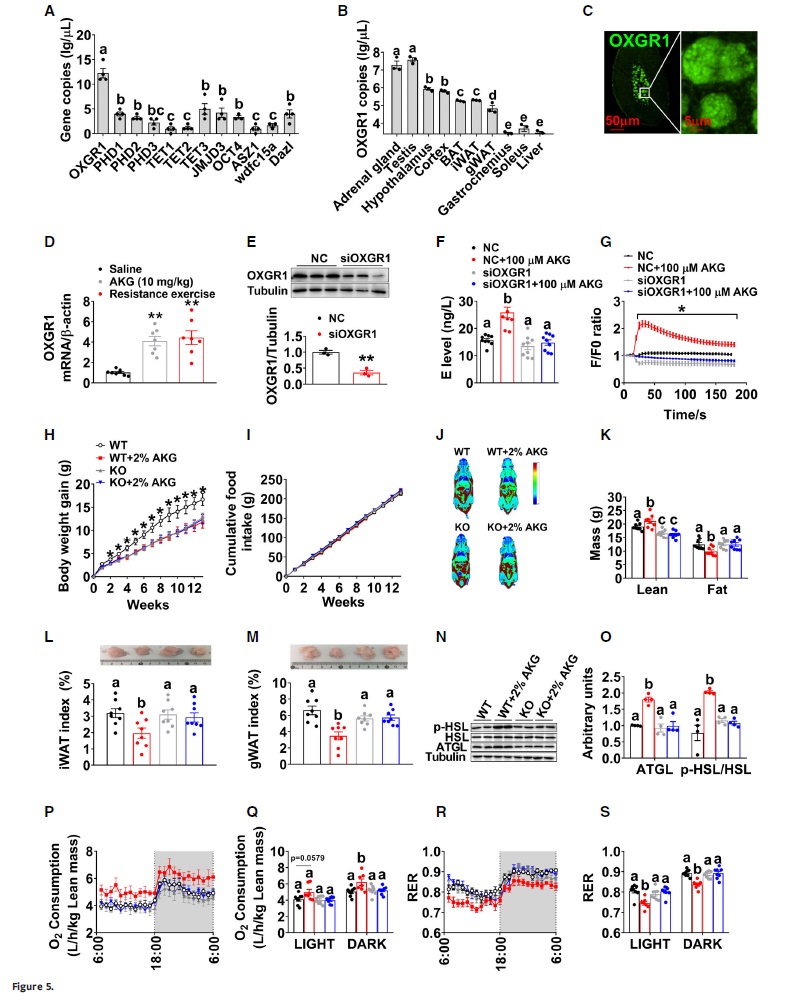
图5. OXGR1是AKG刺激脂肪组织产热和脂解所必需的
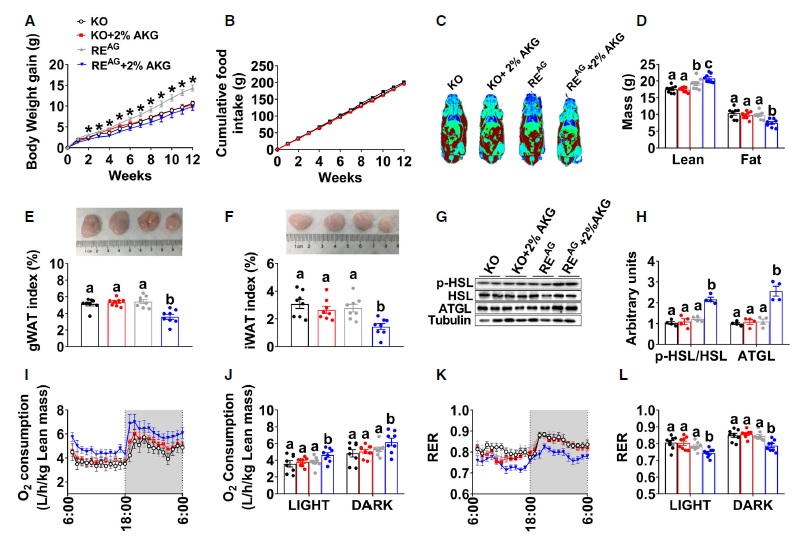
图6. 肾上腺表达的OXGR1介导AKG对产热和脂解的促进作用
OXGR1介导运动产生有益的代谢作用
上述数据表明,运动可以诱导AKG循环水平升高,OXGR1介导AKG的抗肥胖作用。那么运动引起的有益代谢作用是否由OXGR1介导?阻力运动显著提高WT小鼠的血清AKG水平,但在OXGR1KO小鼠中这种刺激作用被减弱(图7H)。运动可有效降低WT对照小鼠体重,而OXGR1的缺失可减弱阻力运动引起的体重下降(图7A和B)。尽管在OXGR1KO和WT对照小鼠中,阻力运动显著降低了脂肪量(图7G),尤其是gWAT和iWAT重量(图7E和F),但相比OXGR1KO小鼠,WT小鼠脂肪量降低程度更明显(图7C),类似的降低也存在于BAT中阻力运动引起的瘦重(图7G)、血清E水平(图7I)、UCP1 mRNA(图7J)和蛋白表达(图7K)、gWAT中ATGL和HSL mRNA表达(图7L)、耗氧量(图7M-N)的增加以及RER的降低(图7O-P)。这些数据共同表明,阻力运动增加了肌肉组织中AKG的分泌,使其与肾上腺OXGR1结合,从而增加脂肪组织的脂解和产热,并阻止DIO。
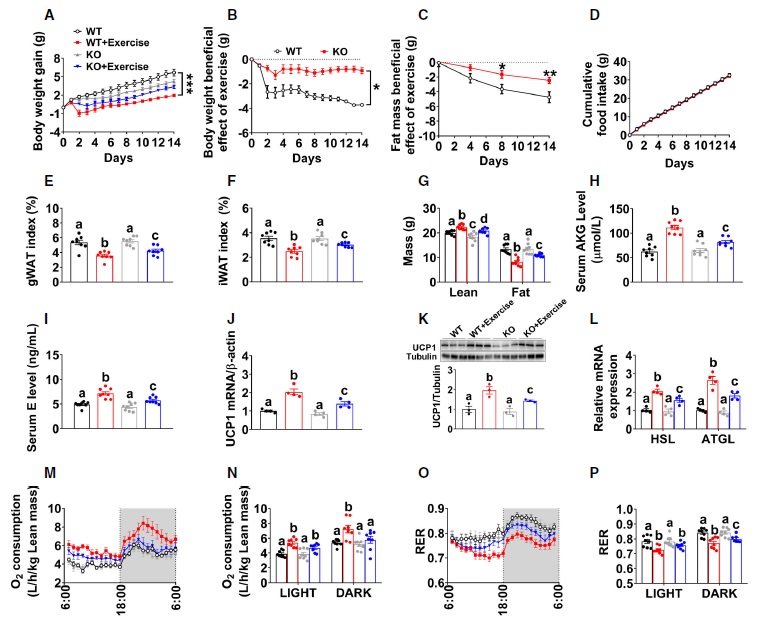
图7. OXGR1是阻力运动的有益代谢作用所必需的
p65/NF-κB炎症通路介导AKG对嗜铬细胞E释放的刺激作用
通过RNA测序研究AKG处理对体外肾上腺嗜铬细胞的转录组变化,对对照组和AKG处理组差异表达的基因进行功能注释发现AKG可激活炎症反应如白细胞介素(IL)通路(图8A)。炎症基因和促炎细胞因子的表达主要受核转录因子κB(NF-κB)调控,而AKG有效地增加B细胞抑制剂α(IkBα,NF-κB的抑制剂)中IκB激酶的磷酸化(IKK,NF-κB的上游激活剂)和kappa光多肽基因增强子的核因子(图8B-C),提示AKG诱导NF-κB活化。此外作者使用siOXGR1生成了OXGR1敲减嗜铬细胞模型证实了NF-κB激活在AKG对嗜铬细胞E释放的刺激过程中具有中介作用。
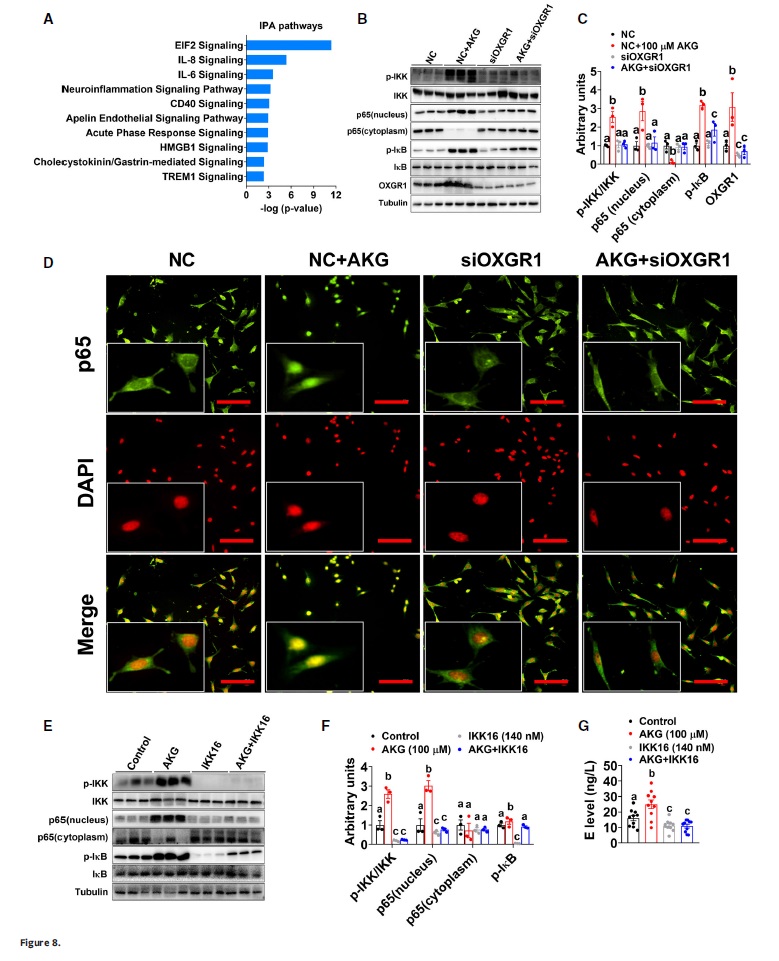
图8. AKG在体外对肾上腺嗜铬细胞E释放的刺激作用需要p65/NF-κB炎症通路
小结
阻力运动可减轻HFD引起的体重增加和肥胖,而这种抗肥胖作用是通过AKG-肾上腺素轴刺激脂肪组织产热和脂解来介导的。通过功能丧失和功能恢复的小鼠模型,发现由肾上腺表达的AKG受体OXGR1对AKG的产热和脂解作用至关重要,也是运动导致的体重减轻和脂肪减少所必需的。体外研究发现AKG对E释放的刺激作用需要激活p65/NF-kB炎症通路。可见AKG是阻力运动抗肥胖作用机制中的重要肌代谢产物,并证明了AKG是一种以前未被重视的全身肾上腺素能信号,AKG作为一种系统衍生的分子来刺激肌肉肥大和脂肪损失,以药理学为靶点的AKG-OXGR1途径可模仿阻力运动对改善体内代谢健康的某些益处,对全身代谢有深远的影响。
参考文献
Yexian Yuan, Pingwen Xu , Qingyan Jiang, Yongliang Zhang & Gang Shu,et al. Exercise-induced a-ketoglutaric acid stimulates muscle hypertrophy and fat loss through OXGR1-dependent adrenal activation. The EMBO Journal (2020) e103304. DOI 10.15252/embj.2019103304.
原文下载,请长按识别下方二维码

精彩推荐
1. Cell Metabolism | 运动调控肠道菌群与代谢物预防糖尿病
2. Nature Medicine | 你离顶级运动员一菌之遥
3. Immunity | lnc-Dpf3抑制CCR7介导的树突状细胞迁移



