文献解读
客户案例 | Cell重磅!代谢物α-KG化身血管 “智能开关”——破解玫瑰痤疮治疗困局
在我们的身体里,代谢物身兼多职,既能在细胞间传递信号,也能像激素一样调控器官功能。若有一种代谢物可以像似“智能开关” 一样精准控制血管舒缩,或许就能成为破解血管异常扩张相关疾病的关键 “钥匙”。
玫瑰痤疮作为常见的慢性面部炎症性皮肤病,持续性红斑与血管异常扩张是其核心困扰,严重影响患者生活质量。当前临床常用的溴莫尼定等药物,虽能暂时收缩血管,却存在疗效短暂、反跳性红斑等棘手副作用。面对这一治疗瓶颈,研究者们不禁思考:是否存在一种内源性代谢物,能通过调控血管平滑肌细胞收缩,从根源上改善红斑症状?
2026年3月,中南大学湘雅医院研究团队在Cell上在线发表了题为“Metabolite-gated vascular contractility switch:OXGR1 activation mechanism enables agonisttherapy for rosacea erythema”的研究文章,采用 “临床发现-机制解析-药物研发-疗效验证” 的全链条研究思路,阐明了α-KG(α-酮戊二酸)通过OXGR1-Gq-MYL9通路调控VSMCs(血管平滑肌细胞)收缩,为理解血管异常提供新视角,并成功开发出选择性OXGR1激动剂A-1,为玫瑰痤疮的治疗提供了新的策略和药物靶点。(麦特绘谱提供Q300全定量代谢组学+有机酸+α-酮戊二酸检测技术服务)
研究思路

图1. 技术路线图
研究结果
1.临床代谢组学检测锁定关键:α-KG是与痤疮红斑相关的保护性代谢物
为了寻找与痤疮红斑相关的代谢物,首先对57名红斑痤疮患者和63名健康对照的血清进行了靶向代谢组学和代谢物分析(麦特绘谱提供的Q300全定量代谢组学+有机酸+α-酮戊二酸检测技术服务)。发现红斑痤疮患者血清中α-酮戊二酸水平显著升高,提示α-KG可能参与红斑的调控过程。
为验证这一猜想,在LL37诱导的玫瑰痤疮样小鼠模型中进行实验,结果显示无论是口服还是局部涂抹α-KG,都能剂量依赖性地缓解小鼠的红斑症状——不仅显著缩小红斑面积、降低红斑评分,还能有效收缩血管直径、减少炎症细胞浸润,且未观察到明显的系统性副作用,证实α-KG是具有治疗潜力的保护性代谢物。
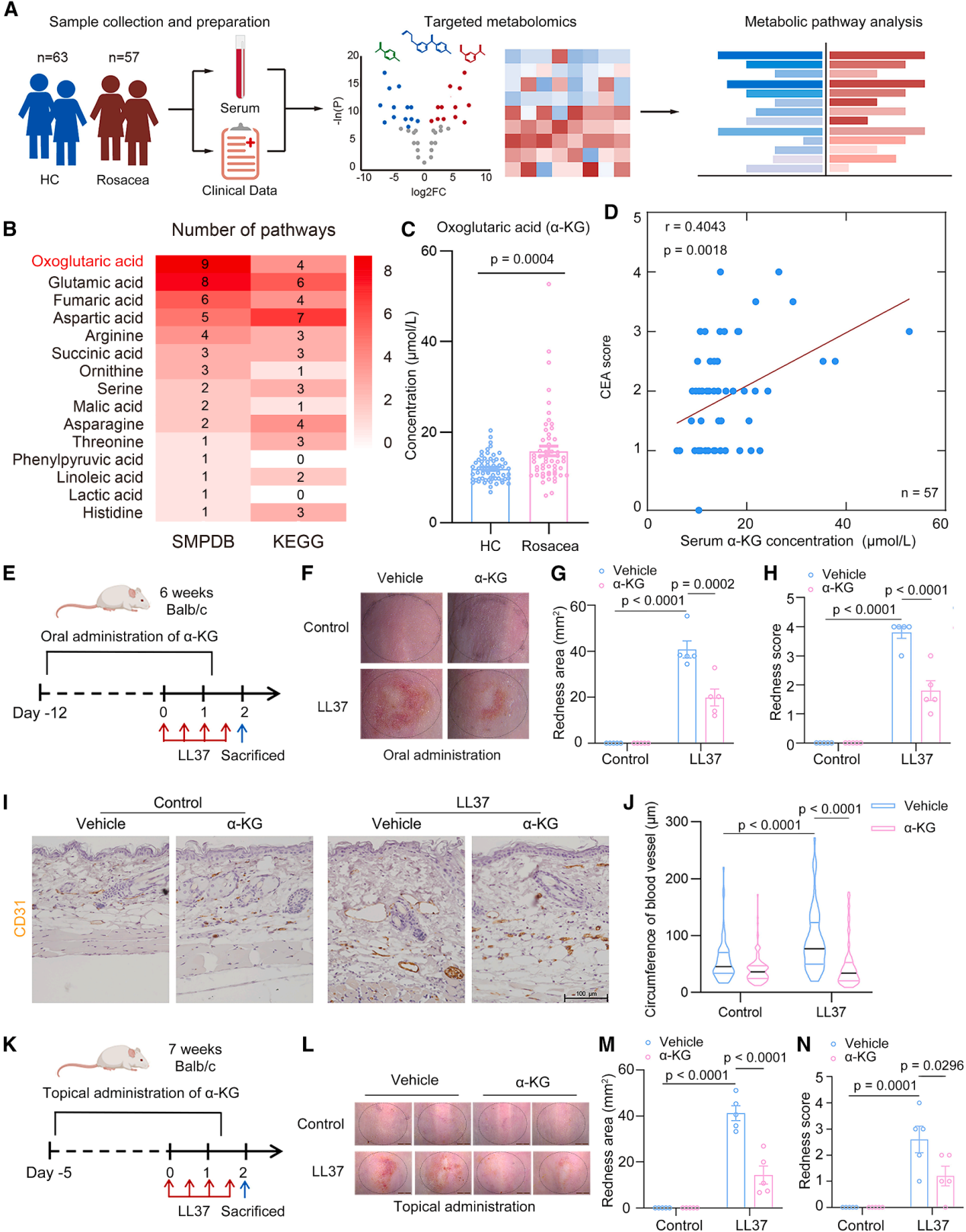
图2. α-KG是玫瑰痤疮的保护性代谢产物
2.靶点与通路明确:α-KG通过OXGR1-Gq-MYL9轴调控血管收缩
为了确定α-KG的潜在作用靶点,对皮肤组织进行了多重免疫荧光染色。结果显示,α-KG的已知受体OXGR1(G蛋白偶联受体)在皮肤中呈现血管样分布模式。共染色实验进一步证实,OXGR1与血管平滑肌细胞(VSMCs)标志物α-SMA共定位,而不与内皮细胞标志物CD31共定位。这一表达模式在人皮肤组织和小鼠皮肤组织中均得到验证,表明OXGR1特异性表达于血管平滑肌细胞,OXGR1可能通过调控血管平滑肌细胞功能来影响血管扩张程度。
为了明确OXGR1在α-KG治疗红斑痤疮中的作用,构建了血管平滑肌细胞特异性Oxgr1基因敲除小鼠,发现α-KG的治疗效果完全消失,证实OXGR1是α-KG发挥作用的必需靶点。
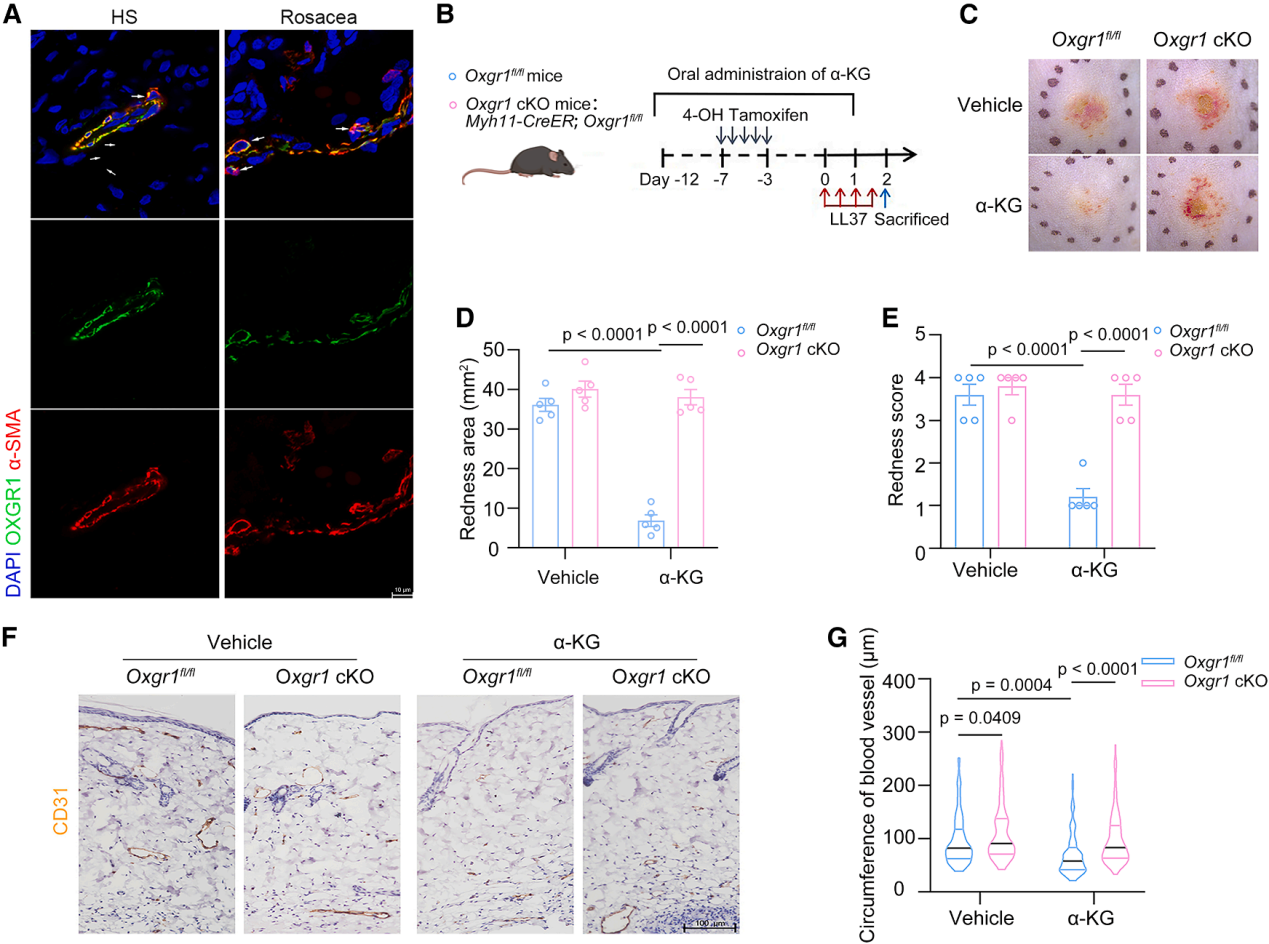
图3. α-KG通过膜受体OXGR1改善玫瑰痤疮样症状
确定了α-KG-OXGR1这一核心轴后,进一步探究其下游信号机制。OXGR1激活后会启动Gq信号通路,进而促进肌球蛋白轻链激酶(MLCK)介导的肌球蛋白轻链9(MYL9)磷酸化——玫瑰痤疮样小鼠的VSMCs中p-MYL9水平显著降低,而α-KG处理能逆转这一现象;当使用MLCK抑制剂(ML-7)或siRNA干扰MLCK表达时,α-KG的血管收缩和红斑缓解效果被阻断。同时,VSMC特异性敲除Gq也会废除α-KG的治疗作用,明确了“α-KG-OXGR1-Gq-MYL9”这一调控血管收缩的核心信号轴。
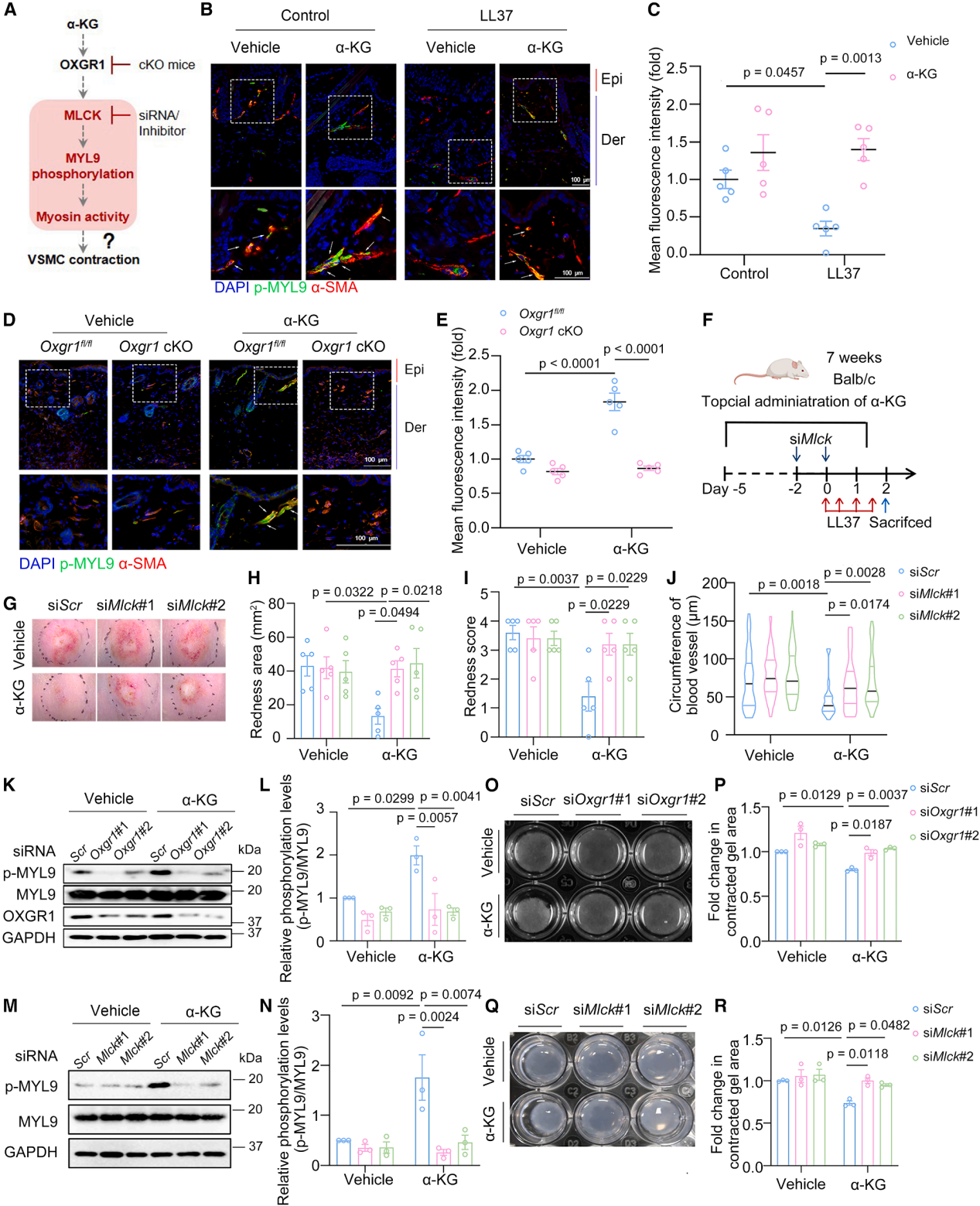
图4. α-KG-OXGR1-MYL9轴预防玫瑰痤疮的异常血管舒张
3.结构生物学揭秘:OXGR1通过双酸性口袋识别配体
进一步阐明OXGR1识别配体的分子基础,利用冷冻电镜解析了OXGR1与α-KG、ITA(衣康酸,另一种内源性OXGR1激动剂)结合的复合物结构,发现OXGR1具有独特的 “双酸性口袋”(SAP简单酸性口袋和CAP复杂酸性口袋):SAP口袋通过 R1103.29-H1143.33-Y2847.35基序与配体的简单羧酸基团结合,CAP口袋则通过Y401.39-Y932.64-R2887.39基序与配体的复杂酸性部分形成氢键和电荷相互作用。
对比分析显示,α-KG与OXGR1的结合更紧密——相较于ITA,α-KG能与OXGR1形成额外的极性相互作用。此外,结构分析还发现OXGR1的激活机制异于经典GPCR,其缺乏典型的W6.48开关残基,依赖 F2546.48的构象变化启动信号传导。
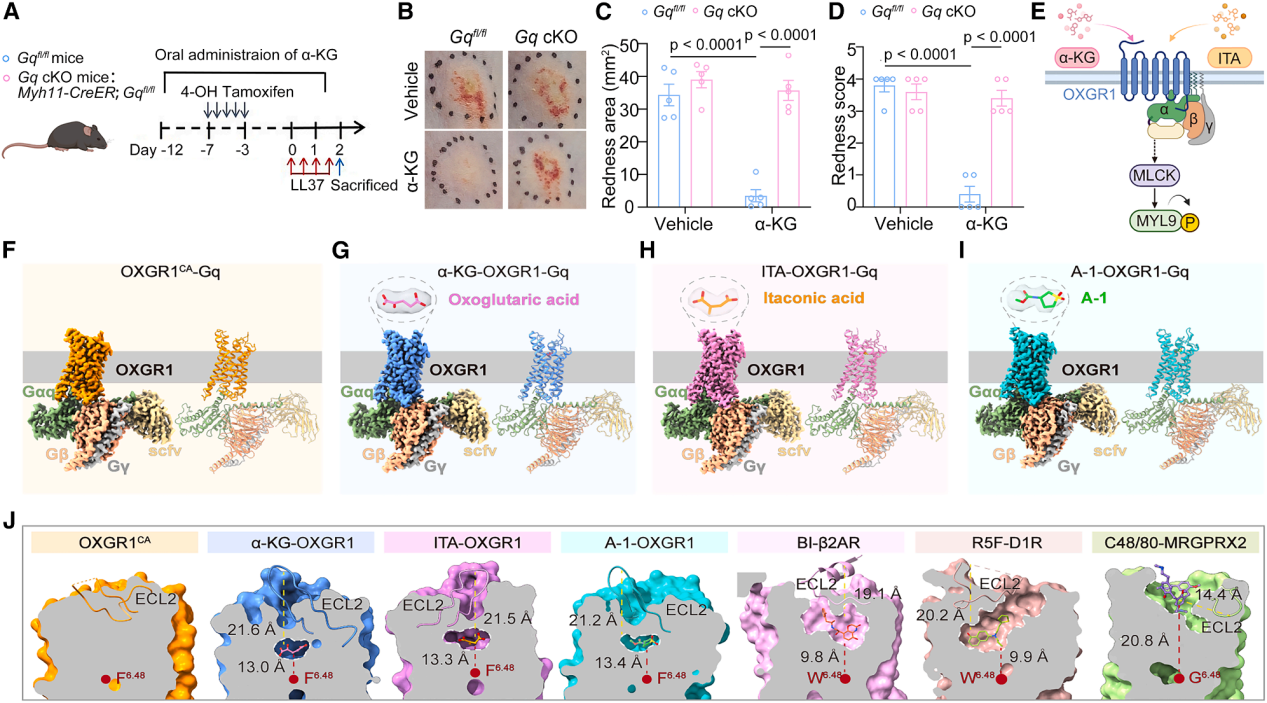
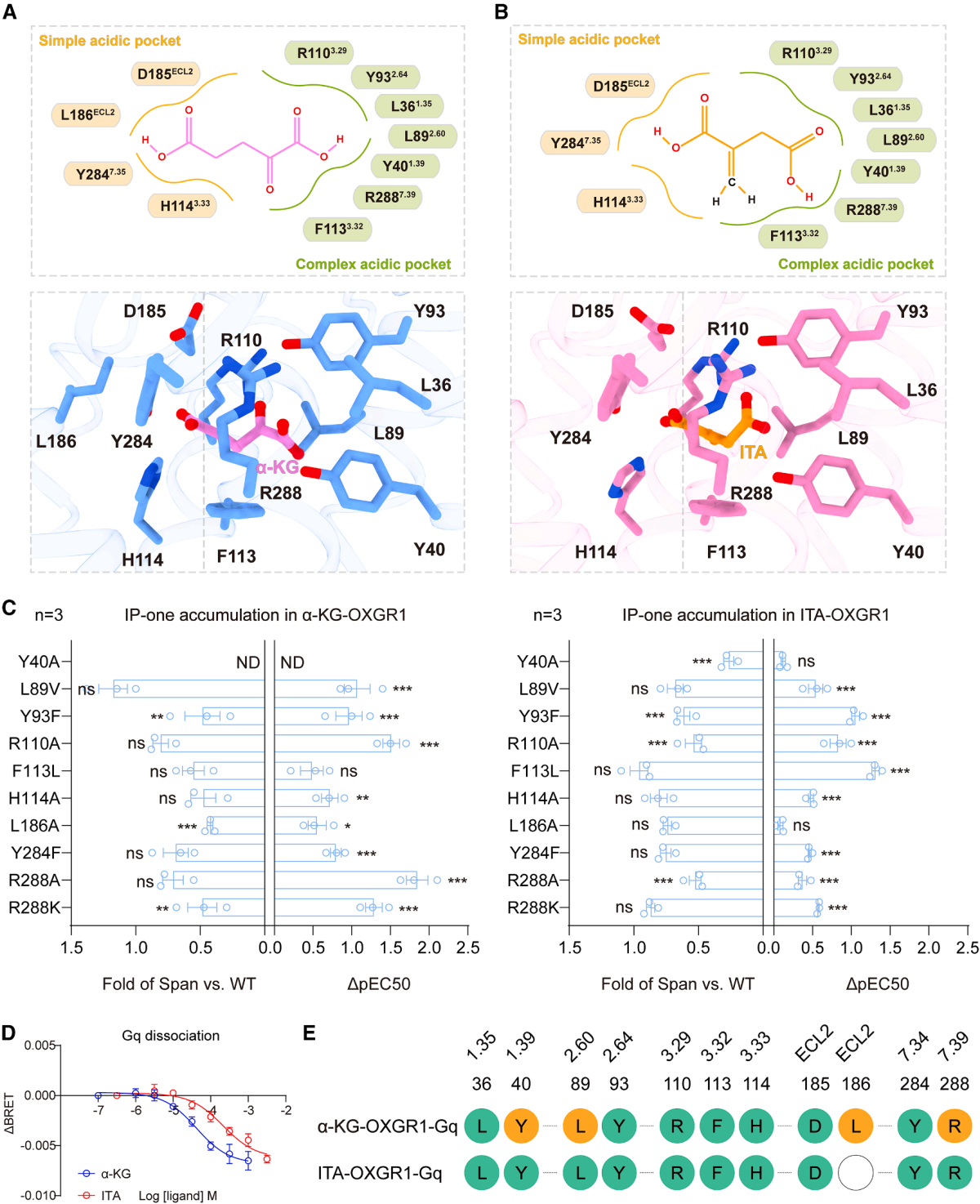
图5. α-KG和ITA结合OXGR1的口袋结构特征
4.药物研发与验证:A-1疗效媲美一线药物且安全性更优
基于OXGR1的结构特征,设计了结构导向的虚拟筛选策略,从化合物库中筛选出3种高活性OXGR1激动剂(A-1、B-2、C-8),其中A-1的表现最为突出,且对OXGR1的同源受体GPR91无明显激活作用,具有高度选择性。
体内外实验验证显示,A-1能有效促进VSMC中MYL9磷酸化和细胞收缩,局部涂抹即可显著缓解小鼠红斑;与临床一线药物溴莫尼定对比发现,A-1的疗效相当,但安全性更优——溴莫尼定长期使用会引发接触性皮炎,停药后还会出现红斑反弹,而A-1不仅无此类副作用,长期给药后仍能持续抑制红斑复发,展现出更优的临床应用潜力。
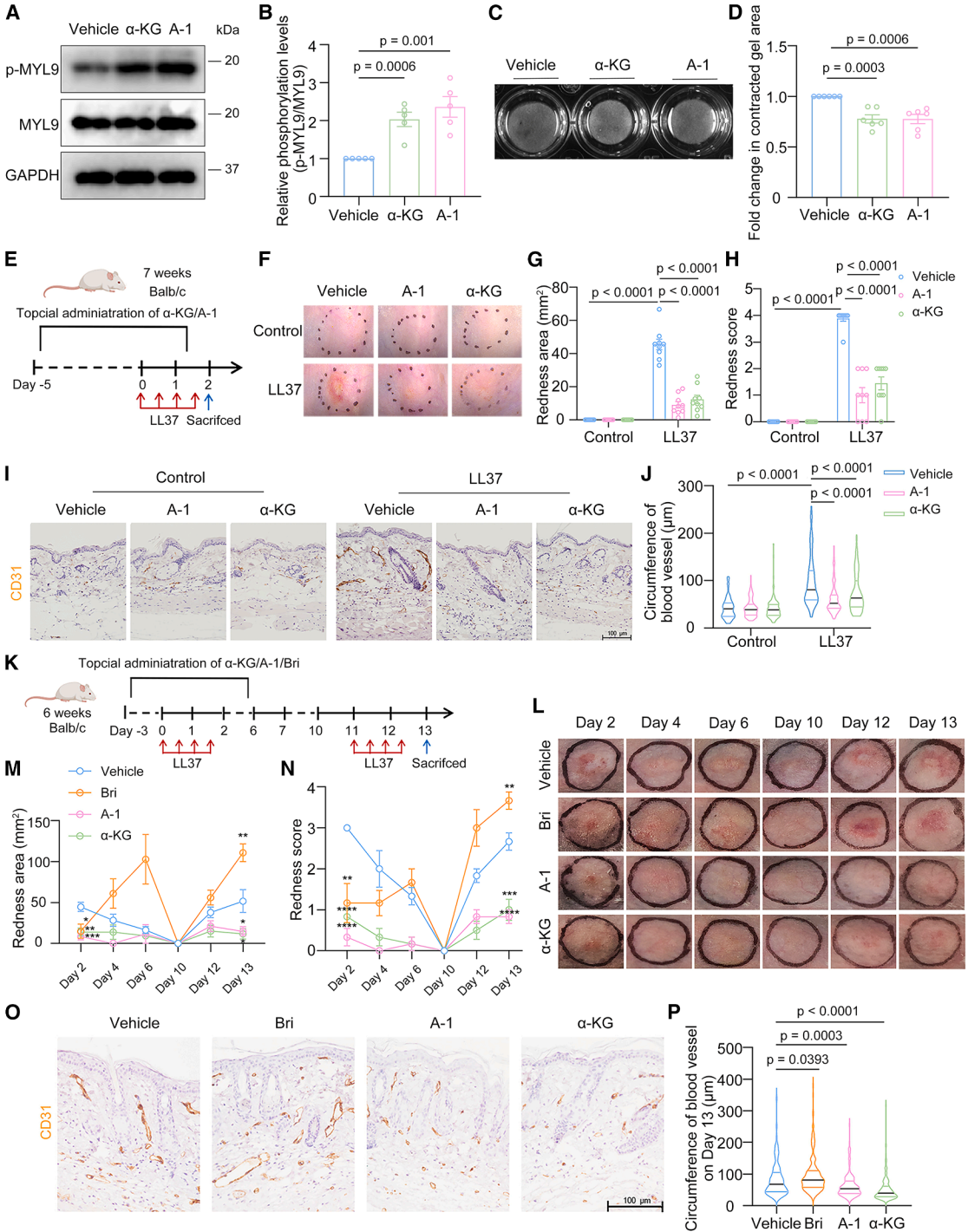
图6. OXGR1激动剂A-1改善玫瑰痤疮症状
研究结论
本研究系统阐明了α-KG在玫瑰痤疮中的作用机制,通过OXGR1-Gq-MYL9轴调控VSMC收缩,揭示了代谢重编程与血管稳态的新型调控关系,阐明了OXGR1独特的双酸性口袋配体识别机制和非经典激活模式,为GPCR家族的结构与功能研究提供了新视角。并成功开发出选择性OXGR1激动剂A-1,为玫瑰痤疮的治疗提供了新的策略和药物靶点。
参考文献
Metabolite-gated vascular contractility switch:OXGR1 activation mechanism enables agonisttherapy for rosacea erythema. Cell. 2026
请扫描二维码阅读原文

绘谱帮你测
本研究中首先基于靶向代谢组学筛选出α-KG这一关键内源性代谢物(麦特绘谱提供),为玫瑰痤疮红斑的病因解析提供了全新代谢视角,也为后续靶点验证、信号通路挖掘及结构导向药物研发奠定了核心基础。
麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱已为数百家三甲医院、科研院所和企业提供多组学一站式整体解决方案,协助客户与合作伙伴发表SCI文章600+篇,累计影响因子6000+,平均IF>10,涵盖Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等顶级期刊。


