文献解读
Cell Death & Differentiation | 肠道胆汁酸调控“肠-脾”免疫轴,开创自身免疫性葡萄膜炎治疗新策略
自身免疫性葡萄膜炎(Autoimmune uveitis, AU)是一种严重影响视力的免疫疾病,传统治疗依赖糖皮质激素,但效果有限,且常伴有全身性副作用。由香港大学医学院、香港浸会大学中医药学院、上海交通大学医学院附属第六人民医院转化医学中心、附属第一人民医院眼科等多家机构共同完成的一项最新研究揭示:肠道来源的次级胆汁酸—猪去氧胆酸(Hyodeoxycholate, HDCA),通过“肠-脾”免疫-代谢通路,调控脾脏红髓巨噬细胞的代谢重塑,从而有效抑制眼部炎症。该研究于2026年3月12日在Cell Death & Differentiation线上正式发表。

原文链接:https://doi.org/10.1038/s41418-026-01696-8
自身免疫性葡萄膜炎的治疗困境
自免性葡萄膜炎是导致工作年龄人群失明的重要原因之一,这种疾病的特点是眼内长期的炎症和免疫系统的失调。目前的主要治疗方法是使用糖皮质激素等免疫抑制药物,虽然可以缓解症状,但长期使用会带来一些严重的副作用,比如股骨头坏死、血糖异常和腹型肥胖等。近年来,新型生物制剂如抗IL-17和抗IL-6受体的单克隆抗体,对银屑病、强制性脊柱炎等自身免疫性炎症显示出一定的治疗潜力,但价格昂贵,很多患者将难以负担。面对这些难题,急需开发出既能有效控制病情、副作用少,又具有较高性价比的新型治疗方案,以改善患者的生活质量。
突破性发现:HDCA与油酸的双重缺失
研究团队通过对90名参与者(包括60名AU患者和30名健康对照)的血清样本进行定量代谢组学分析,首次揭示了AU患者独特的代谢异常特征。结果显示,猪去氧胆酸(HDCA)是AU患者中下降最为显著的胆汁酸类代谢物(见图1)。此外,患者血清中的不饱和脂肪酸,特别是油酸(C18:1n9)水平也出现显著下降。这种代谢紊乱在实验性自身免疫性葡萄膜炎(EAU)小鼠模型中得到完美重现,证实HDCA和油酸的缺乏是葡萄膜炎相关炎症的特征性代谢标志物,为疾病的早期诊断和干预提供了新的生物标志物和潜在治疗靶点。
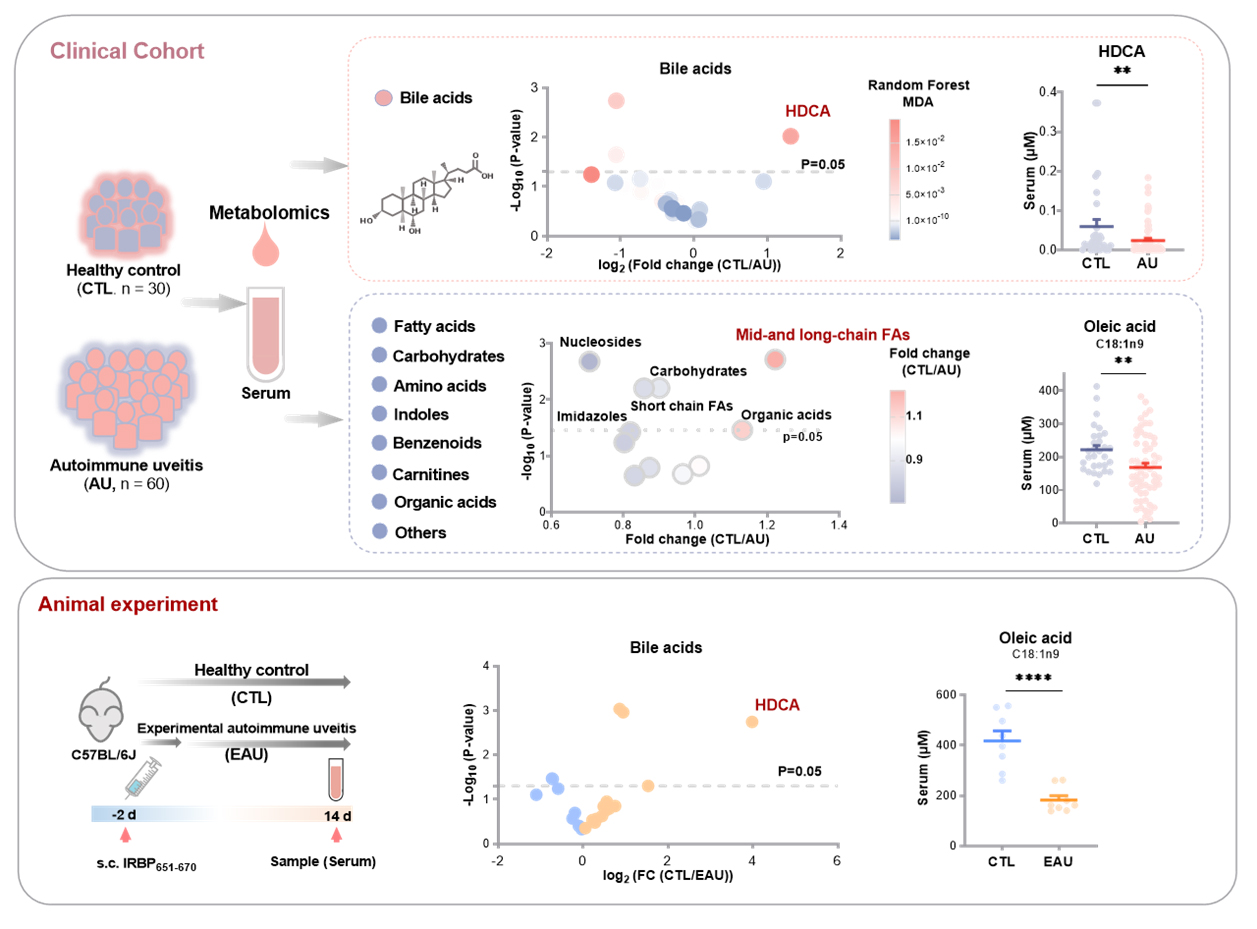
图1. AU患者和EAU小鼠模型血清中HDCA和油酸水平显著降低
HDCA重构“肠-脾”免疫代谢轴,精准抑制眼部炎症
研究团队发现口服HDCA能够显著减轻EAU小鼠的疾病严重程度。HDCA治疗不仅降低了炎症的临床评分,改善了眼部组织病理变化,如视网膜折叠、新生毛细血管生成及炎症免疫细胞浸润,还减少了IL-1β、IL-6、IL-17a等炎症因子,同时升高了抗炎因子IL-10的水平(见图2)。眼底成像和光学相干断层扫描(OCT)证实,HDCA治疗显著减轻了视盘炎症和视网膜组织损伤。
在细胞机制方面,HDCA治疗显著抑制了眼部有害的Th17细胞的分化,同时促进巨噬细胞向抗炎的M2表型极化。这一抗炎效果在两种不同遗传背景的小鼠(C57BL/6J和BALB/c)中均得到验证,显示出HDCA具有广泛的抗炎潜力。
团队发现,HDCA的核心治疗机制在于通过维持脾脏红髓巨噬细胞(RPMs)的数量,同时抑制法尼醇X受体(FXR)的活性,激活SREBP1c依赖的脂肪酸合成途径,从而促进油酸的生成。这些油酸通过血液循环和免疫细胞的调节,远程作用于眼部,调控局部免疫反应,形成一条全新的“肠道-脾脏-眼”免疫代谢轴。这一重要发现揭示了HDCA在调节免疫平衡中的关键作用,为实现眼部炎症的精准干预提供了新的理论基础和潜在的治疗靶点。
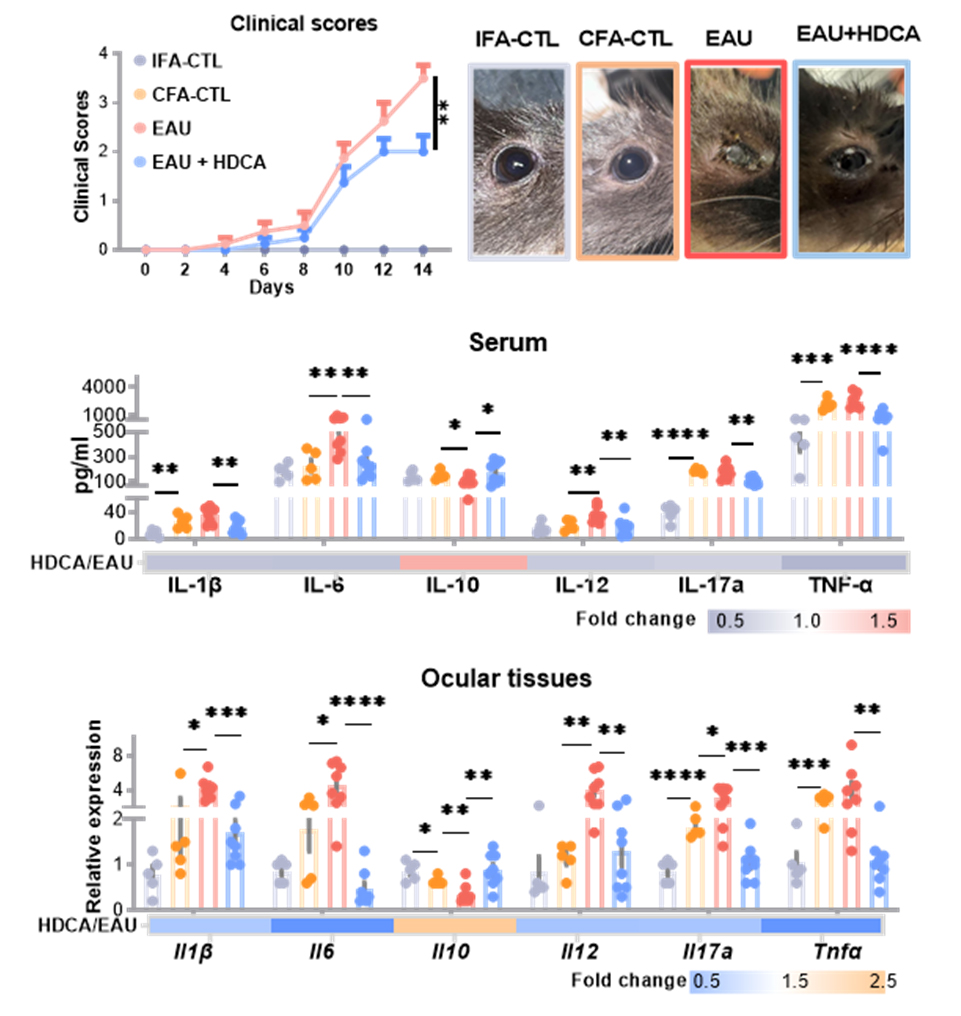
图2. HDCA治疗显著减轻EAU小鼠眼部炎症
机制创新——脾脏红髓巨噬细胞是免疫调控的核心代谢枢纽
巨噬细胞是固有免疫系统的重要组成部分,主要分为两类:一类是由单核细胞来源的巨噬细胞,另一类是组织驻留的巨噬细胞。组织驻留巨噬细胞在维持组织稳态和调控免疫耐受方面发挥着关键作用。然而,其功能或代谢异常(如异常呈递自身抗原)可能导致过度促使CD4+T细胞分化为致病性Th17细胞,从而加重自身免疫疾病。
作为全身最大的外周免疫器官,脾脏包含多种类型的组织驻留巨噬细胞,其中以红髓巨噬细胞(RPMs)为本研究的核心靶细胞。研究团队发现,口服HDCA能够在脾脏中高效富集,选择性作用于RPMs(见图3)。HDCA通过抑制法尼醇X受体(FXR),激活依赖SREBP1c的脂肪酸合成酶(FASN),从而促进油酸的内源性合成。当RPMs被清除后,HDCA调节免疫反应和恢复油酸水平的能力明显减弱,证实RPMs在远程调控免疫和代谢中的关键作用。
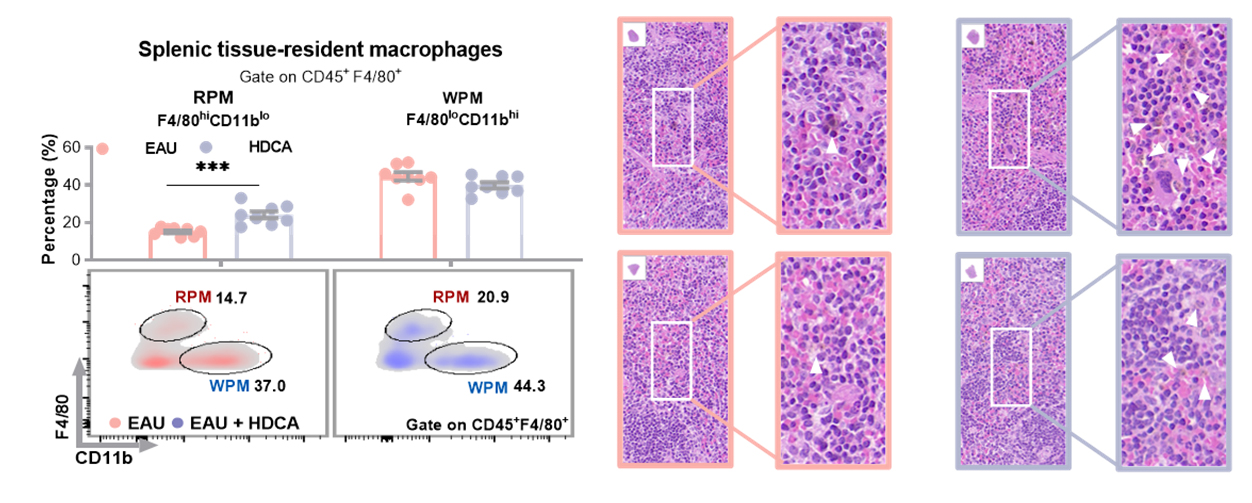
图3. HDCA治疗后脾脏红髓巨噬细胞富集
进一步研究发现,来自脾脏红髓巨噬细胞(RPMs)的油酸通过血液循环输送到眼部,发挥双重的免疫调节作用:一方面抑制致病性Th17细胞的分化,减少炎症反应;另一方面促使巨噬细胞向抗炎的M2表型极化,增强免疫抑制能力(见图4)。值得注意的是,尽管大量研究表明,富含油酸的地中海饮食可以显著降低自身免疫性疾病的发病风险,但外源性油酸难以特异性靶向调控RPMs,从而无法复制HDCA所引导的脂肪酸重编程过程。这也解释了为什么直接补充油酸的治疗效果远不如HDCA显著,进一步凸显了本研究所揭示的机制的创新价值和潜在优势。
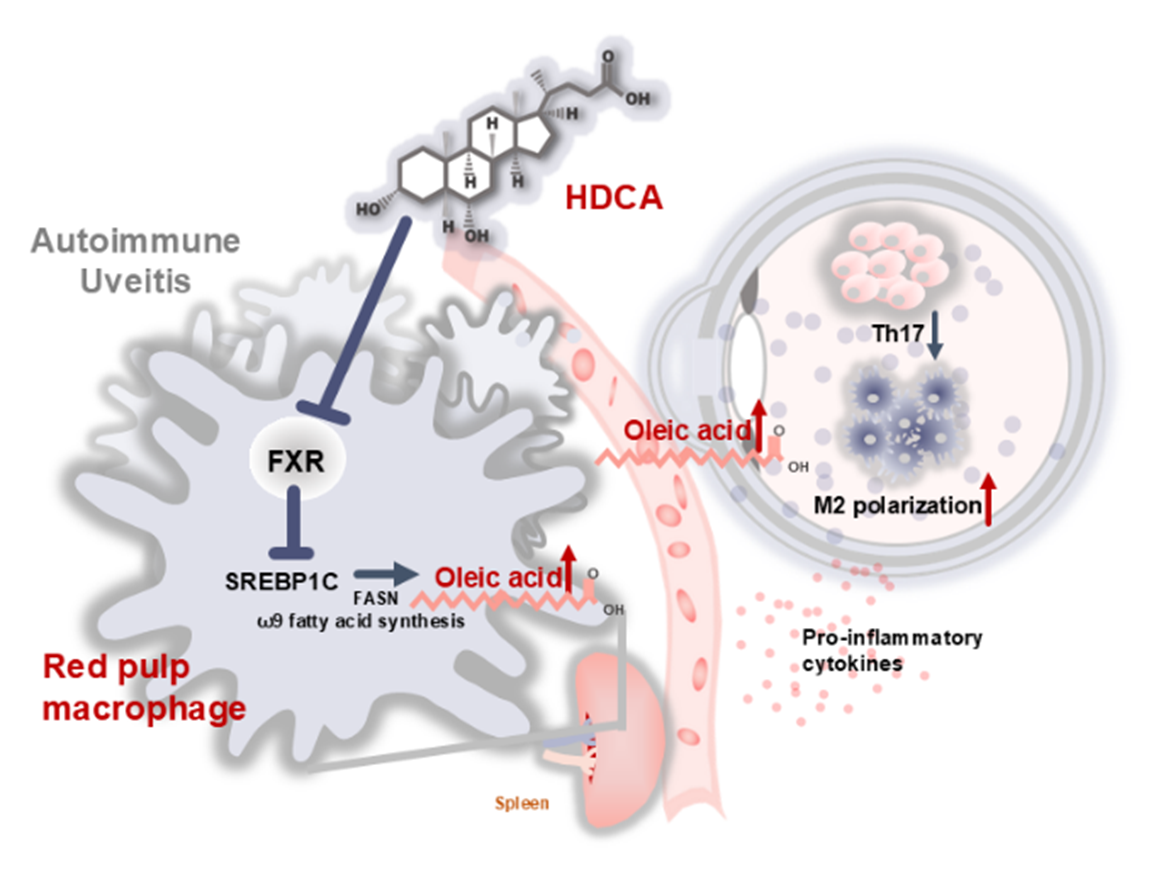
图4. “脾-眼”免疫代谢轴调控示意图
【治疗优势】
HDCA作为一种内源性次级胆汁酸,具有独特的治疗优势:
1、精准靶向:HDCA通过“肠-脾”免疫代谢轴实现远程调控,主要作用于脾脏中的红髓巨噬细胞,避免了传统免疫抑制药物可能带来的全身性免疫抑制副作用。
2、双重作用机制:HDCA既促进抗炎的油酸合成,又能够扩增脾脏红髓巨噬细胞的数量,通过细胞调控和代谢产物调节两条途径协同发挥治疗效能。
3、高安全性:作为人体内天然存在的代谢产物,HDCA具有良好的生物相容性。前期研究已证实其安全性,不会像游离脂肪酸直接补充那样引发全身代谢紊乱或其他副作用。
4、用药便捷:HDCA可口服给药,大大提高了慢性病患者的用药依从性。作为小分子化合物,其生产工艺成熟、成本较低,有望显著减轻患者的经济负担。
目前,研究团队正积极推进HDCA的临床前安全性评估和制剂研发,力争尽早启动临床试验,将这一基于内源性代谢物的创新疗法惠及更多葡萄膜炎患者及其他自身免疫性疾病患者。
【延伸阅读】
1、猪胆酸:猪,为何天生“吃不胖、不得糖尿病”?
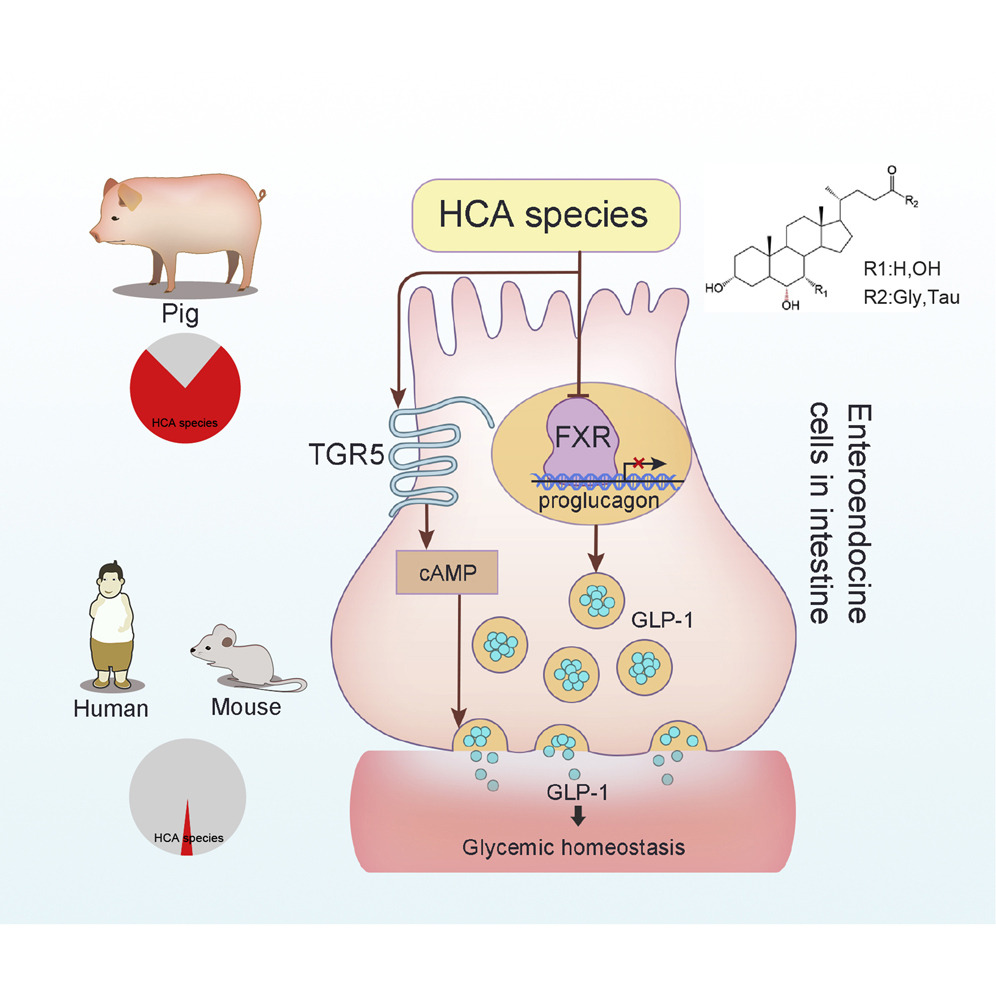
在中医传统中,猪胆常被用于清热解毒,而现代科学研究则揭示了其更深层的健康价值。早在2020年,贾伟教授团队发现,猪胆汁中的主要活性成分——猪胆酸及其衍生物,在糖脂代谢调控中扮演着至关重要的角色,通过作用于TGR5和FXR两种关键受体,显著促进GLP-1的分泌,从而帮助维持血糖稳定。这一成果不仅解释了猪为何对高热量饮食诱导的2型糖尿病具有天然抵抗力,也为人类糖尿病风险预测和治疗方案创新提供了全新视角。相关论文发表于Cell Metabolism “纪念胰岛素发现100周年”专刊。(点击查看完整解读)
2、猪去氧胆酸:从控糖到护肝的“新使命”
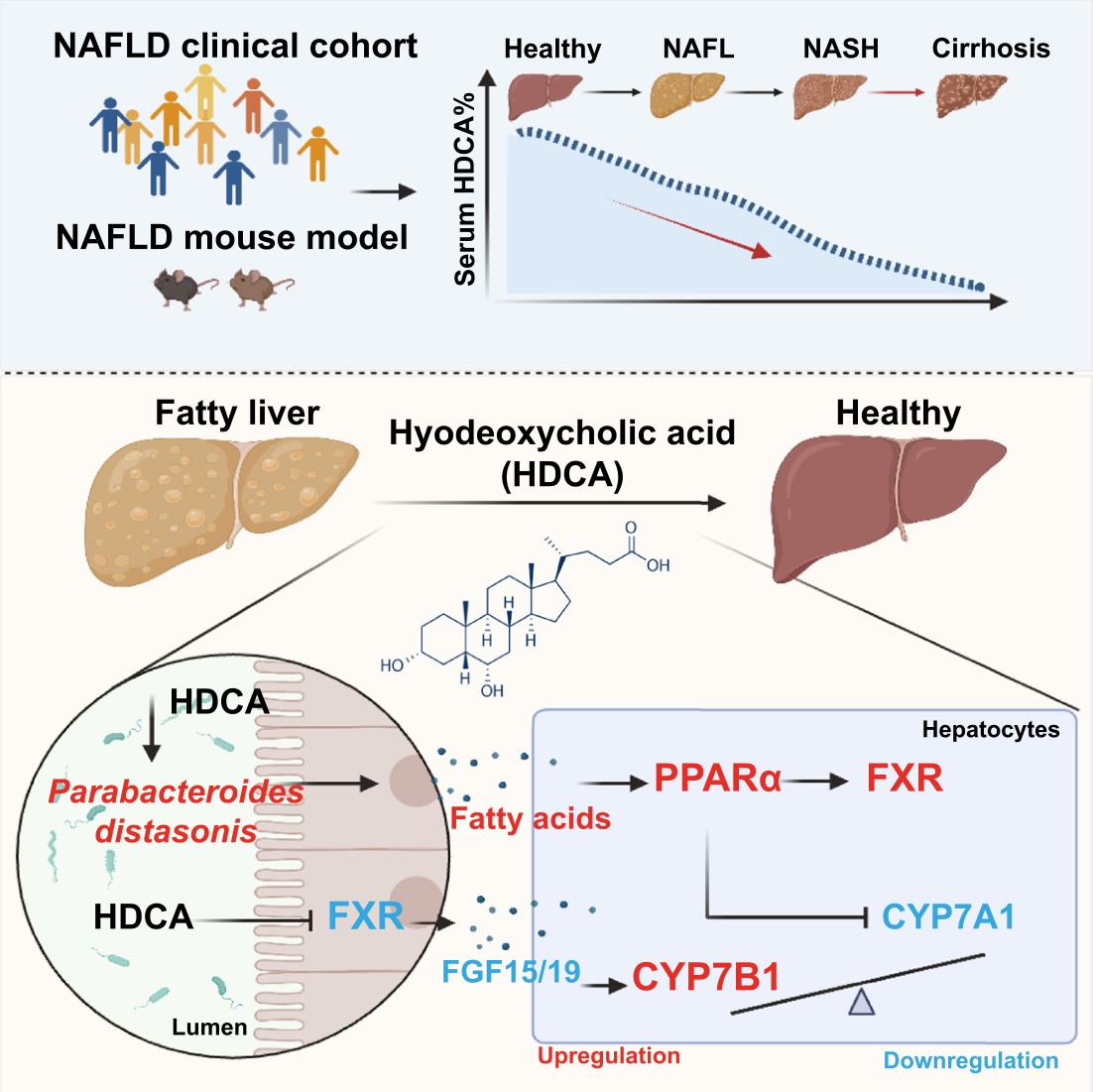
随着研究不断深入,贾伟教授团队于2023年再度取得突破,立足肠-肝轴调控网络,首次揭示猪去氧胆酸缓解非酒精性脂肪性肝病的新机制——内源性HDCA通过肠(肠道菌群与肠道FXR信号通路)-肝脏(CYP7B1、PPARα)轴缓解肝脏脂质堆积,HDCA改变肠道菌群提供有利于P. distasonis生长的微环境,产生γ-亚麻酸并通过PPARα信号传导抑制肝脏CYP7A1经典胆汁酸合成通路,从而改善非酒精性脂肪性肝病,为脂肪肝的防治提供了关键靶点与干预策略。(点击查看完整解读)
• 本研究由香港大学医学院/上海交通大学医学院附属第六人民医院贾伟教授、上海交通大学医学院附属第一人民医院杨晓璐教授、香港浸会大学中医药学院吕爱平教授、意大利罗马第二大学实验医学系Gerry Melino教授作为共同通讯作者完成。
• 香港浸会大学中医药学院李忆涛、香港大学医学院郑维嘉为本文共同第一作者。
• 该研究获得了香港研究资助局General Research Fund及上海市科学技术委员会上海市科技创新行动计划等项目的资助。
麦特绘谱持续护航顶刊研究
麦特绘谱依托贾伟教授团队的前沿科研积累,构建Q200、Q300、Q500、Q1000、QL1000和胆汁酸、短链脂肪酸、色氨酸及吲哚衍生物、多胺和TMAO类等各类小分子代谢物、非靶向代谢组学和同位素示踪代谢流技术等共50+系列检测方法,为全球科研与临床客户提供精准、高效的多组学解决方案。
凭借稳定、精准、高覆盖的技术优势,麦特绘谱已持续助力国内外科研团队在Cell, Nature, Science, Cancer Cell, Cell Metabolism等顶尖期刊发表高分论文数百篇。从机制发现到靶点验证,从基础研究到临床转化,麦特绘谱将继续以精准代谢组学为引擎,推动疾病早筛、机制研究与创新疗法不断突破,为守护国人健康持续贡献力量。

参考文献
[1]Li Y, Zheng W, Ma J, et al. Gut-derived hyodeoxycholate reprograms the spleen-eye immunometabolic axis to suppress autoimmune uveitis. Cell Death Differ. Published online March 11, 2026. doi:10.1038/s41418-026-01696-8
[2]Kuang J, Wang J, Li Y, et al. Hyodeoxycholic acid alleviates non-alcoholic fatty liver disease through modulating the gut-liver axis. Cell Metab. 2023;35(10):1752-1766.e8. doi:10.1016/j.cmet.2023.07.011
[3] Zheng X, Chen T, Jiang R, et al. Hyocholic acid species improve glucose homeostasis through a distinct TGR5 and FXR signaling mechanism. Cell Metab. 2021;33(4):791-803.e7. doi:10.1016/j.cmet.2020.11.017


